一 : 乙肝表面抗原定量测定的方法学验证


乙肝表面抗原的ELISA法定量分析
姓名 Z P
学号 0925400072
班级 09
指导老师
方法学验证 级医学检验本科二班 沈 富 兵
二〇一三年四月
乙肝表面抗原定量测定的方法学验证 作者:ZP(成都医学院检验医学院09级医学检验本科二班,610500)
【摘要】 目的 用福州蓝图生物工程有限公司出品的乙肝表面抗原ELISA法定量分析试剂盒对乙肝表面抗原定量测定的方法进行验证,以判断是否能用于教学以及临床分析。方法 运用ELLISA法定量测定乙肝表面抗原,应用试剂盒HBsAg标准从浓度为8ng/ml的2倍稀释的6个浓度梯度,根据OD值绘制标准曲线再计算相对回收率和板内和板间精密度,通过资料数据综合分析。结果 HBsAg线性较好,其准确度、精密度、LOD值均在正常范内。结论 ELISA法定量检测HBsAg能较准确、快速地反映体内乙肝病毒复制情况,可以用于教学以及临床分析。
【关键词】 乙肝表面抗原 方法学验证 标准曲线 精密度 ELLISA
病毒性肝炎中乙型肝炎的危害较大,我国是病毒性乙型肝炎的高发流行区,普通人群的乙型肝炎病毒(hepatitis B virus,HBV)感染率接近60%,约占世界HBV携带者的1/3。乙型肝炎病毒的病原体不仅具有传染性,还可能导致发展成肝硬化,甚至肝癌,所以乙型肝炎病毒的早期、准确、定量检测对乙型肝炎临床诊断、疗效观察及预防具有重要的意义。酶免分析法HBV—EIA是HBV抗原和抗体最常用的检测技术,其方法简便、价廉,适合一般实验室推广,其中酶联免疫吸附技术(enzyme linked immunosorbent assay, ELISA)目前应用最为广泛,它常用聚苯乙烯为固相载体,使其与待测标本中的相应抗体或抗原结合,然后加酶标记的抗原或抗体,再加底物显色,最后根据色泽深浅来推算待测抗原或抗体的含量。此方法特异性高,有效测定范围可达到20500 ng/ml,且酶免疫法有标记的试剂比较稳定并且无放射线危害等优点。
我们采用对已知抗体浓度的样品进行ELISA的定量检测,通过对其数据的分析来验证ELISA法最乙肝表面抗原定量检测的准确性和可靠性,以衡量其实用性。
1 材料与方法
1.1 材料
1.1.1 试剂盒
乙肝表面抗原ELISA法定量分析试剂盒,福州蓝图生物工程有限公司出品。
1.1.2 仪器及酶标板
酶标仪:Bio-Rad 680;洗板机:Bio-Rad 1575;超纯水系统:Millipore Elix;电热恒温培养箱(DNP-9052):上海精宏实验设备有限公司。
1.1.3 溶液配制
⑴0.01M pH7.4的PBS缓冲液:
称取8g NaCl、0.2g KCl、1.44g Na2HPO4和0.24g KH2PO4, 溶于800ml蒸馏水中,用HCl调节溶液的pH值至7.4,最后加蒸馏水定容至1L即可。 ⑵质控品:
用PBS缓冲液将标准品配制成6、3、1.5ng/ml三个质控品,每质控品1ml。
首先取450μl的8ng/ml的标准品到C1号EP管中再向其中加入150μl的PBS缓冲液,即配制成了6ng/ml的质控品,再取300μl C1号EP管内的溶液到C2号EP管内,再向C2号管内加入300μl的缓冲液混匀。即配制成了3ng/ml的质控品。接着取300μl C2号管内的液体到C3号EP管内,再加入300μl的缓冲液混匀,即配制成了1.5ng/ml的质控品。具体方法如下图1
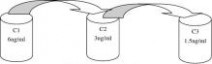
图1
1.2 检测方法
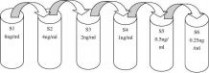
1.2.1 标准曲线各浓度的配制 ⑴用PBS缓冲液将标准品配制成8、4、2、1、0.5、0.25ng/ml。 ⑵先取6个EP管分别标记为对应的浓度。 ⑶取400μl标准品于标记为?的EP管中,再取200μl?号管内液体于?号管内再向?号管中加入200μl的缓冲液混匀,即配制成了浓度为4ng/ml的标准品。 ⑷再从?号管内取200μl的液体到?号管内,接着取200μl的缓冲液到?号管内混匀,即配制成了2ng/ml的标准品。 ⑸从?号管内取200μl的标准品到④号管内,再向④号管内加入200μl的缓冲液混匀,即配制成了1ng/ml的标准品。 ⑹用同样的方法,配制好浓度分别为0.5ng/ml、0.25ng/ml.的标准品体积分别为200μl、200μl、400μl备用。具体方法如下图2
图2
1.2.2 测定方法
⑴取出试剂盒中已包被酶标板,取出板条,在相应孔中加入已配制好的系列
标准品、质控品及空白对照;
图3
注:双线框区域为标准品,浓度依次为8、4、2、1、0.5、0.25ng/ml,三线框区域为质控品,浓度依次为6、3、1.5ng/ml,粗框区域为空白对照加入的是PBS缓冲液,每个孔内加入的均是50μl。
⑵37℃温育30min,洗板4次;
⑶加入酶标抗体,生物素二抗,50μl/孔; ⑷37℃温育30min,洗板4次;
⑸加入A、B液,50μl/孔,37℃温育15分钟; ⑹加入终止液,50μl/孔。 1.3 标准曲线制作及结果计算
⑴酶标板放入酶标仪,盖上盖子;
⑵在电脑上打开Microplate Manager 5.2软件;
⑶选择450nm波长(参照波长630nm),设置LAYOUT和报告模式,测定各孔吸收值;
⑷输入标准品各浓度值,以双对数法制备标准曲线,获取各孔的浓度值,打印标准曲线图和计算结果。 1.4 统计学方法
用Microsoft Excel处理实验数据。
2 结果
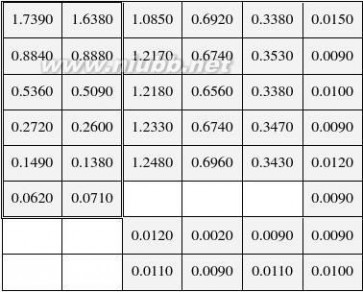
2.1 测得的OD值如下表

二 : 1个有争议的话题:乙肝表面抗原定量的意义
| 1个有争议的话题:乙肝表面抗原定量的意义 | |
|
三 : 乙肝表面抗原定量测定的方法学验证


乙肝表面抗原的ELISA法定量分析
姓名 Z P
学号 0925400072
班级 09
指导老师
方法学验证 级医学检验本科二班 沈 富 兵
二〇一三年四月
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
乙肝表面抗原定量测定的方法学验证 作者:ZP(成都医学院检验医学院09级医学检验本科二班,610500)
【摘要】 目的 用福州蓝图生物工程有限公司出品的乙肝表面抗原ELISA法定量分析试剂盒对乙肝表面抗原定量测定的方法进行验证,以判断是否能用于教学以及临床分析。[www.61k.com]方法 运用ELLISA法定量测定乙肝表面抗原,应用试剂盒HBsAg标准从浓度为8ng/ml的2倍稀释的6个浓度梯度,根据OD值绘制标准曲线再计算相对回收率和板内和板间精密度,通过资料数据综合分析。结果 HBsAg线性较好,其准确度、精密度、LOD值均在正常范内。结论 ELISA法定量检测HBsAg能较准确、快速地反映体内乙肝病毒复制情况,可以用于教学以及临床分析。
【关键词】 乙肝表面抗原 方法学验证 标准曲线 精密度 ELLISA
病毒性肝炎中乙型肝炎的危害较大,我国是病毒性乙型肝炎的高发流行区,普通人群的乙型肝炎病毒(hepatitis B virus,HBV)感染率接近60%,约占世界HBV携带者的1/3。乙型肝炎病毒的病原体不仅具有传染性,还可能导致发展成肝硬化,甚至肝癌,所以乙型肝炎病毒的早期、准确、定量检测对乙型肝炎临床诊断、疗效观察及预防具有重要的意义。酶免分析法HBV—EIA是HBV抗原和抗体最常用的检测技术,其方法简便、价廉,适合一般实验室推广,其中酶联免疫吸附技术(enzyme linked immunosorbent assay, ELISA)目前应用最为广泛,它常用聚苯乙烯为固相载体,使其与待测标本中的相应抗体或抗原结合,然后加酶标记的抗原或抗体,再加底物显色,最后根据色泽深浅来推算待测抗原或抗体的含量。此方法特异性高,有效测定范围可达到20500 ng/ml,且酶免疫法有标记的试剂比较稳定并且无放射线危害等优点。
我们采用对已知抗体浓度的样品进行ELISA的定量检测,通过对其数据的分析来验证ELISA法最乙肝表面抗原定量检测的准确性和可靠性,以衡量其实用性。
1 材料与方法
1.1 材料
1.1.1 试剂盒
乙肝表面抗原ELISA法定量分析试剂盒,福州蓝图生物工程有限公司出品。
1.1.2 仪器及酶标板
酶标仪:Bio-Rad 680;洗板机:Bio-Rad 1575;超纯水系统:Millipore Elix;电热恒温培养箱(DNP-9052):上海精宏实验设备有限公司。
1.1.3 溶液配制
⑴0.01M pH7.4的PBS缓冲液:
称取8g NaCl、0.2g KCl、1.44g Na2HPO4和0.24g KH2PO4, 溶于800ml蒸馏水中,用HCl调节溶液的pH值至7.4,最后加蒸馏水定容至1L即可。 ⑵质控品:
用PBS缓冲液将标准品配制成6、3、1.5ng/ml三个质控品,每质控品1ml。
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
首先取450μl的8ng/ml的标准品到C1号EP管中再向其中加入150μl的PBS缓冲液,即配制成了6ng/ml的质控品,再取300μl C1号EP管内的溶液到C2号EP管内,再向C2号管内加入300μl的缓冲液混匀。[www.61k.com]即配制成了3ng/ml的质控品。接着取300μl C2号管内的液体到C3号EP管内,再加入300μl的缓冲液混匀,即配制成了1.5ng/ml的质控品。具体方法如下图1
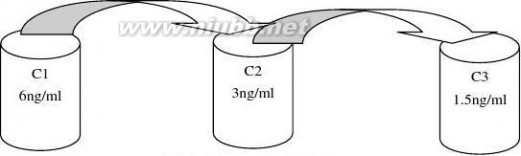
图1
1.2 检测方法

1.2.1 标准曲线各浓度的配制 ⑴用PBS缓冲液将标准品配制成8、4、2、1、0.5、0.25ng/ml。 ⑵先取6个EP管分别标记为对应的浓度。 ⑶取400μl标准品于标记为?的EP管中,再取200μl?号管内液体于?号管内再向?号管中加入200μl的缓冲液混匀,即配制成了浓度为4ng/ml的标准品。 ⑷再从?号管内取200μl的液体到?号管内,接着取200μl的缓冲液到?号管内混匀,即配制成了2ng/ml的标准品。 ⑸从?号管内取200μl的标准品到④号管内,再向④号管内加入200μl的缓冲液混匀,即配制成了1ng/ml的标准品。 ⑹用同样的方法,配制好浓度分别为0.5ng/ml、0.25ng/ml.的标准品体积分别为200μl、200μl、400μl备用。具体方法如下图2
图2
1.2.2 测定方法
⑴取出试剂盒中已包被酶标板,取出板条,在相应孔中加入已配制好的系列
标准品、质控品及空白对照;
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
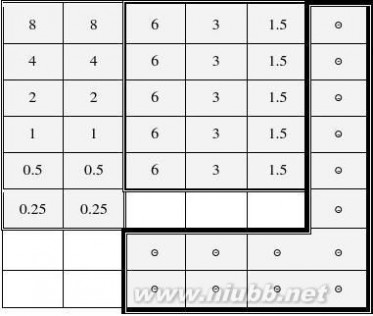
图3
注:双线框区域为标准品,浓度依次为8、4、2、1、0.5、0.25ng/ml,三线框区域为质控品,浓度依次为6、3、1.5ng/ml,粗框区域为空白对照加入的是PBS缓冲液,每个孔内加入的均是50μl。[www.61k.com]
⑵37℃温育30min,洗板4次;
⑶加入酶标抗体,生物素二抗,50μl/孔; ⑷37℃温育30min,洗板4次;
⑸加入A、B液,50μl/孔,37℃温育15分钟; ⑹加入终止液,50μl/孔。 1.3 标准曲线制作及结果计算
⑴酶标板放入酶标仪,盖上盖子;
⑵在电脑上打开Microplate Manager 5.2软件;
⑶选择450nm波长(参照波长630nm),设置LAYOUT和报告模式,测定各孔吸收值;
⑷输入标准品各浓度值,以双对数法制备标准曲线,获取各孔的浓度值,打印标准曲线图和计算结果。 1.4 统计学方法
用Microsoft Excel处理实验数据。
2 结果
2.1 测得的OD值如下表
61阅读提醒您本文地址:
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
图4
注:图4与图3相对应
2.2 标准曲线
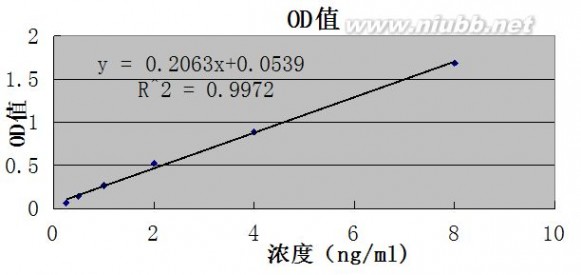
图5
由上图可得出如下结论:
标准曲线以浓度为横坐标,以测得的OD值为纵坐标。(www.61k.com]由对应浓度和OD值得出的散点连成一条直线后,散点基本都在直线上,说明散点的线性非常好。在以后检测乙肝表面抗原浓度的时候可以根据测出的OD值在标准曲线上找出对应的浓度。
2.3 准确度(回收率)计算
各质控品高中低三个浓度平均回收率分别为92.59%、100.887%、93.68% 都在正常范围内 如表1所示。
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
ELISA法检测VEGFR2-Fc的回收率
准确度(回收率)计算VEGFR2-Fc (ng/ml)
6 6 6 6 6 3 3 3 3 3 1.5 1.5 1.5 1.5 1.5
测定值(ng/ml)
回收率(%)
平均回收率RR(%) 92.59
SD(%)
4.998 5.637 5.642 5.715 5.787 3.093 3.005 2.918 3.005 3.112 1.377 1.450 1.377 1.421 1.401 83.3 93.95 94.033 95.25 96.45 103.1 100.167 97.267 100.167 103.733 91.8 96.667 91.8 94.733 93.4 表1
5.30
100.887 2.60
93.68 2.07
2.4 精密度计算
2.4.1 板内精密度
板内精密度质控品各浓度组的RSD都小于15%,精密度良好,如表2所示。(www.61k.com]
板内精密度
VEGFR2-Fc 测定值 测定值 (ng/ml)
测定值
测定值 测定值
1 2 3
5.642 2.918 1.377
4
5.715 3.005 1.421 表2
5
5.787 3.112 1.401
S?
5.694±0.318 3.027±0.078 1.405±0.031
RSD(%)
63 1.5
4.998 3.093 1.377
5.637 3.005 1.450
5.5852.577 2.210
2.4.2 板间精密度
板间各组浓度质控品RSD都小于15%,说明板间精密度达到标准。如表3所示。
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
板间精密度
VEGFR2-Fc 测定值 测定值 测定值 测定值
(ng/ml)
6
6 6 3 3 3 1.5 1.5 1.5
4.998 5.471 5.773 3.093 2.815 2.886 1.377 1.226 1.665
5.637 5.423 5.674 3.005 3.335 3.344 1.450 1.257 1.243
5.642 5.674 5.782 2.918 3.187 3.118 1.377 1.227 1.236
5.715 5.323 5.547 3.005 3.221 3.234 1.421 1.564 1.541 表3
测定值 5.787 5.746 5.667 3.112 2.933 2.997 1.401 1.334 1.320
S?5.694±0.318 5.5274±0.177 5.689±0.096 3.027±0.078 3.098±0.216 3.116±0.182 1.405±0.031 1.322±0.142 1.401±0.192
RSD(%) 5.585 3.202 1.687 2.577 6.972 5.841 2.210 10.741 13.704
2.5 检测限(LOD)计算:
取空白孔的OD值的均数加2倍标准差。(www.61k.com) 空白孔的OD值的均数=0.0098 空白孔的OD值的标准差=0.0028 LOD=0.0098+2*0.0028=0.0154
3 讨论
通过图4、图5和表1、表2、表3可知本次实验的准确度、板内精密度、板间精密度、LOD值都复合实际,且各数据都趋于理想,对此我们做出分析: HBsAg是乙肝病毒感染后最早出现的血清标志物之一,因此HBsAg的检测是诊断肝炎病毒感染的重要依据。而针对这项检测的检测方法的灵敏度与高特异性的高低以及二者的结合程度是影响检验结果的重要因素,直接关系到临床诊断和用药,所以对HBsAg的检测方法的建立和方法的验证是实验成败的关键所在。
本实验以HBsAg测定为例,为了对乙肝表面抗原ELISA法定量进行分析的方法学建立与验证,以确认ELISA法定量检测HBsAg能否较准确、快速地反映体内乙肝病毒复制情况。按试剂说明书严格操作的同时做标准曲线。本实验用的试剂盒采用双抗体夹心法酶联免疫吸附试验(ELISA)。往预先包被人乙肝病毒表面抗原(HBsAg)捕获抗体的包被微孔中,依次加入标本、标准品、HRP标记的检测抗体,经过温浴并彻底洗涤。用底物TMB显色,TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
人乙肝病毒表面抗原(HBsAg)呈正相关。[www.61k.com)用酶标仪在450nm波长下测定吸光度(OD值),计算样品浓度。本实验严格按试剂说明书操作的同时运用计算机软件和酶标仪,测得了OD值且绘制出了标准曲线。
本实验采用双抗体夹心法酶联免疫吸附试验(ELISA),通过倍比稀释来完成其定量检测。其中,标准品的浓度依次为:8、4、2、1、0.5、0.25ng/ml,每个浓度设置两个孔,共十二个孔;质控品的浓度依次为:6、3、1.5ng/ml,每个浓度设置五个孔,共十五个孔。往标准品、质控品依次加入标本、标准品、HRP标记的检测抗体,而阴性对照加入等量PBS,经过温浴并彻底洗涤。用底物TMB显色,TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。用酶标仪在450nm波长下测定吸光度(OD值),计算质控品的准确度、板内精密度、板间精密度、LOD值。
本实验是设计精密,操作简便、快捷。主要是通过对质控品的准确度、板内精密度、板间精密度、LOD值的计算和根据标准品的OD值得出的标准曲线,以确认ELISA法定量检测HBsAg能否较准确、快速地反映体内乙肝病毒复制情况。
如图5所示,标准曲线相关系数为0.9985,接近于1,即相关性良好。方法准确度(accuracy),一般用相对回收率表示,表明用该方法测得的生物样品中待测药物的浓度与其真实浓度的接近程度,由表1可得出相对回收率符合参考值85%~115%,所以该测定方法比较准确。
方法精密度(precision),一般用RSD表示,对于ng/ml级水平的RSD一般应≤15%。由表2板内精密度和表3板间精密度可知,板内精密度完全符合要求,板间精密度基本符合要求。
61阅读提醒您本文地址:
检测限LOD,又称方法的灵敏度,由计算得LOD=0.0154,说明本分析方法对于低浓度样品的检测灵敏度高。
根据流行病学调查, 我国人群乙型病毒肝炎感染率达10% 左右,乙肝的实验诊断对于其治疗及预防有重要参考意义。ELLISA适用于乙肝表面抗原的定量测定, 其优点是快速、方便、操作简单, 且灵敏度相对于其他方法较高, 自20世纪70年代以来, 许多高灵敏度的测定方法应用于临床免疫学检测, 特别是酶联免疫法( ELLISA法)应用最广,其解决了低浓度HBsAg的定量检测问题, 能够及时
乙肝表面抗原定量 乙肝表面抗原定量测定的方法学验证
有效的测定出乙肝表面抗原含量,对临床诊断和用药提供有力的依据。[www.61k.com)
综上所述,通过实验对HBsAg的准确度、板内精密度、板间精密度、LOD值的评价和分析,证实该定量检测方法,具有高灵敏度和高特异性,能够满足临床检测和教学的要求。
参考文献
[1] 李金明,王露楠,徐锡霞,等.室内质量控制对乙型肝炎表面抗原准确的影响[J].中华检验医学杂志,2001,24(4) :255.
[2] 施纪文,徐简华,温惠萍.ELISA法和胶体金免疫层析法检测乙肝表面抗原的比较[J].现代检验医学杂志,2005,20(5):49.
[3] 章敏,万唐,彭慧中,等.前S2、前S1抗原与乙肝病毒标志物的相关性探讨[J].实验与检验医学,2009,27(6):609.
[4] 陈慧英,张锦锋,岑小鹏,等..ELISA检测乙型肝炎HBsAg室内质控血清的试剂和使用[J].上海医学检验杂志,2000,15(4):203-205.
[5] 周小辉,周元平,姚春平.血清HBV DNA复制与慢性乙型炎肝脏损伤程度的研究[J].中国现代医学杂志,2000,13(4):133-135.
[6] 梅小平,李健,曾跃.乙型肝炎病毒DNA水平与临床的关性分析[J].中华肝脏病杂志, 2004,16(5):19-21.
[7] 赵公之.乙型肝炎病毒DNA检测与临床 [J].中国实用医药,2006,9(4):87-88.
61阅读提醒您本文地址:
本文标题:乙肝表面抗原定量-乙肝表面抗原定量测定的方法学验证61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1