一 : 原子结构》优秀课件PPT
化学:1.1《原子结构》 优秀课件PPT(人教版选 修3)
引言
化学研究的是构成宏观物体的物质。
一、研究物质的组成与结构
二、研究物质的性质与变化
思考
二者的关系如何?古希腊的“原性论” 哲学和我国古代的炼丹术士认为“吞金可长 生” 自然哲学,对这两者的关系是如何认定的?
思考与交流
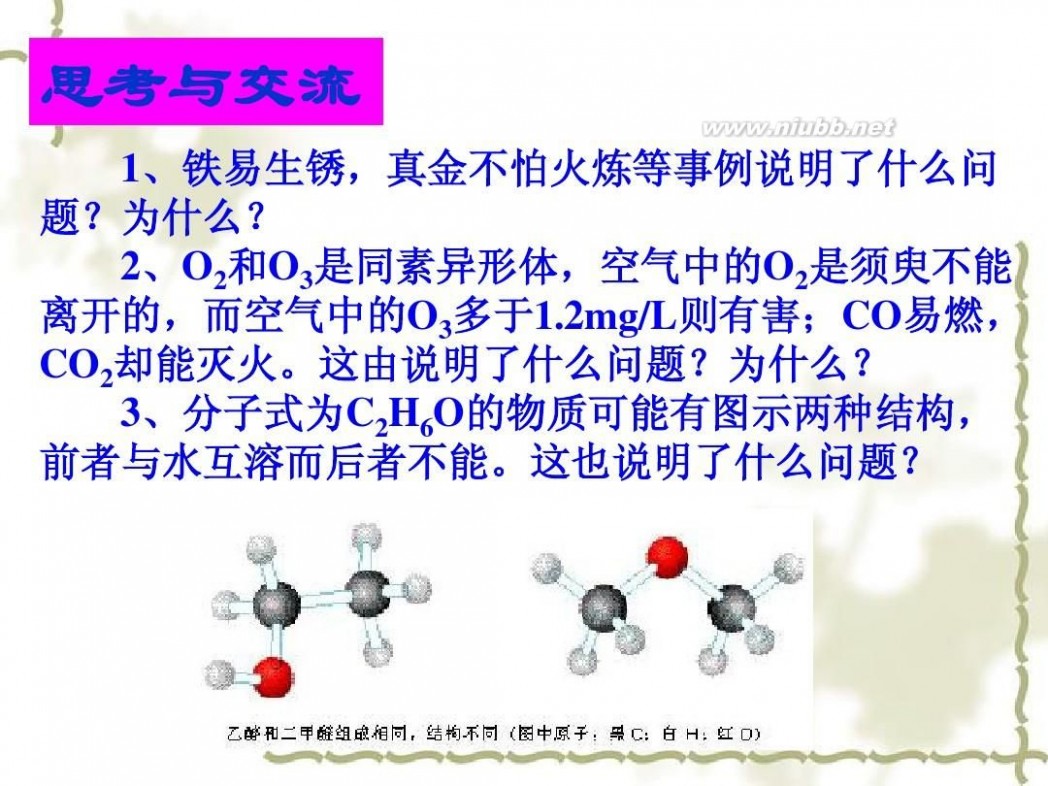
1、铁易生锈,真金不怕火炼等事例说明了什么问 题?为什么? 2、O2和O3是同素异形体,空气中的O2是须臾不能 离开的,而空气中的O3多于1.2mg/L则有害;CO易燃, CO2却能灭火。这由说明了什么问题?为什么? 3、分子式为C2H6O的物质可能有图示两种结构, 前者与水互溶而后者不能。这也说明了什么问题?
思 考 与 交 流
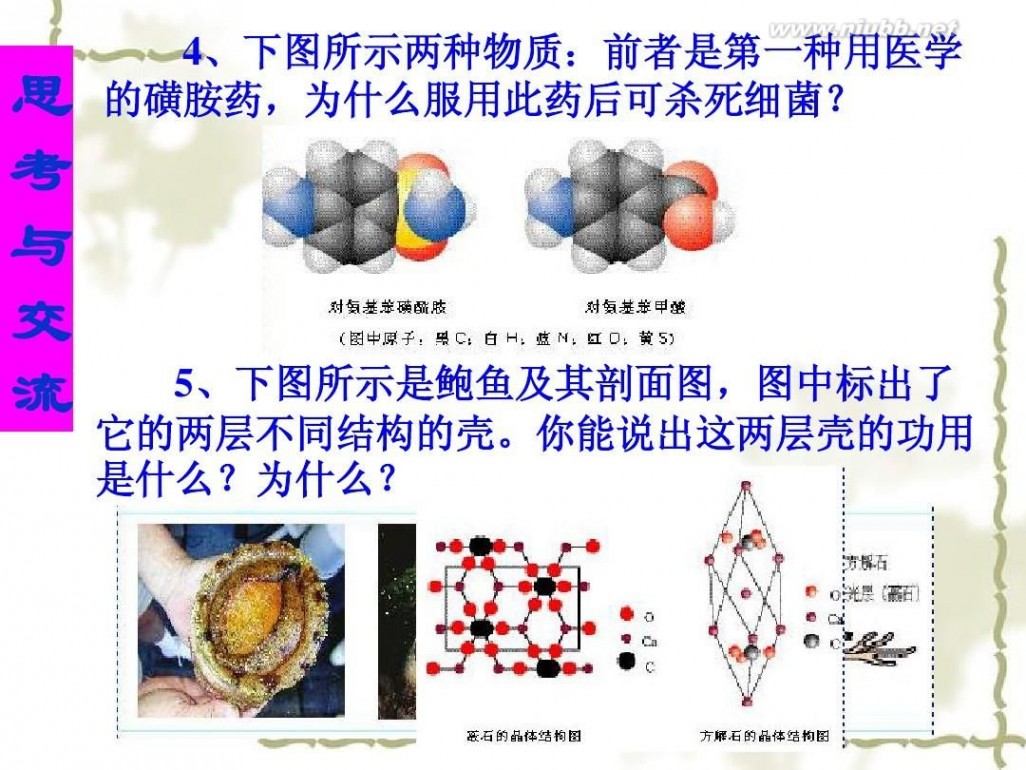
4、下图所示两种物质:前者是第一种用医学 的磺胺药,为什么服用此药后可杀死细菌?
5、下图所示是鲍鱼及其剖面图,图中标出了 它的两层不同结构的壳。你能说出这两层壳的功用 是什么?为什么?
引言
原子结构 分子结构 晶体结构
结 构
决定
性 质
宇宙大爆炸
宇宙大爆炸
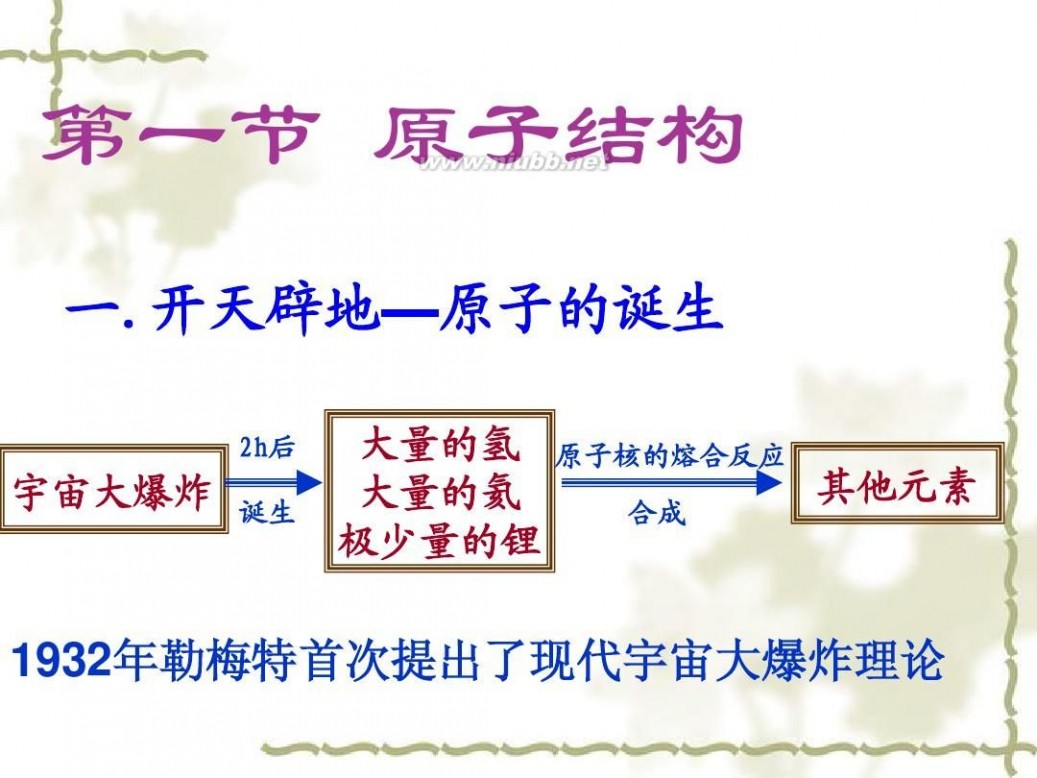
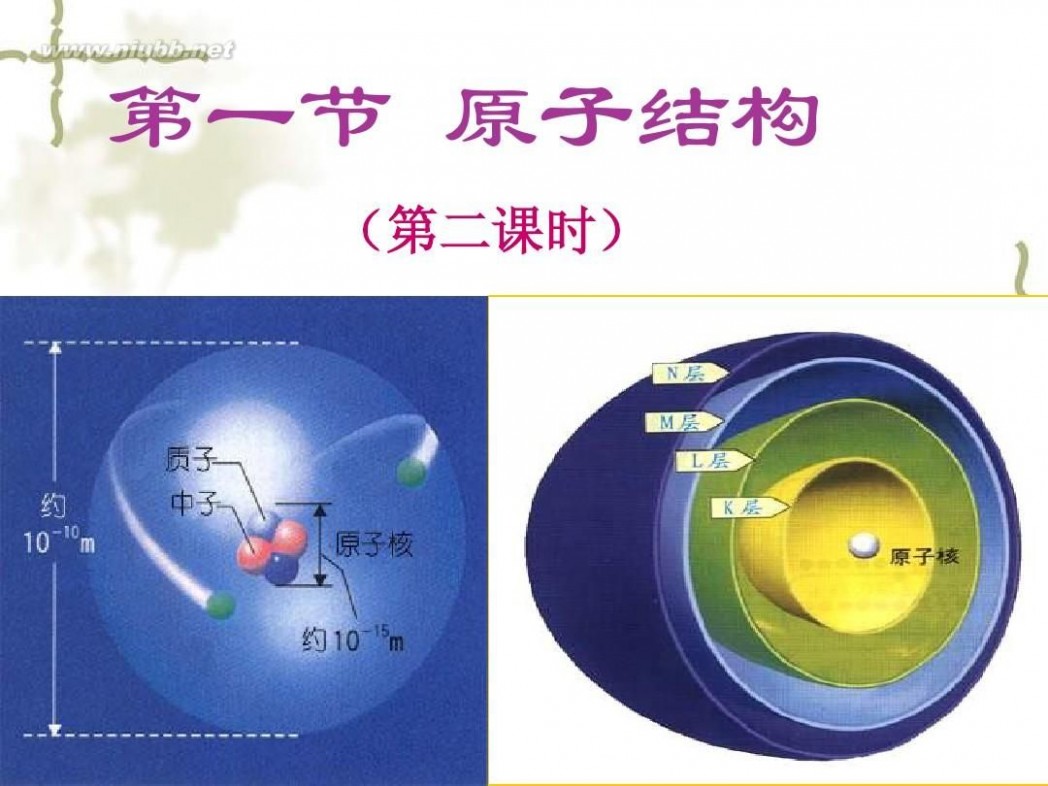
第一节 原子结构
一.开天辟地—原子的诞生
2h后
宇宙大爆炸
诞生
大量的氢 大量的氦 极少量的锂
原子核的熔合反应 合成
其他元素
1932年勒梅特首次提出了现代宇宙大爆炸理论
思考与交流
有谁知道宇宙中最丰富的元素是那一种? 宇宙年龄有多大?地球年龄有多大? 回 答
阅读课本后回答:氢元素宇宙中最丰富 的元素占88.6%(氦1/8),另外还有90多 种元素,宇宙年龄距近约140亿年,地球年龄 已有46亿年。
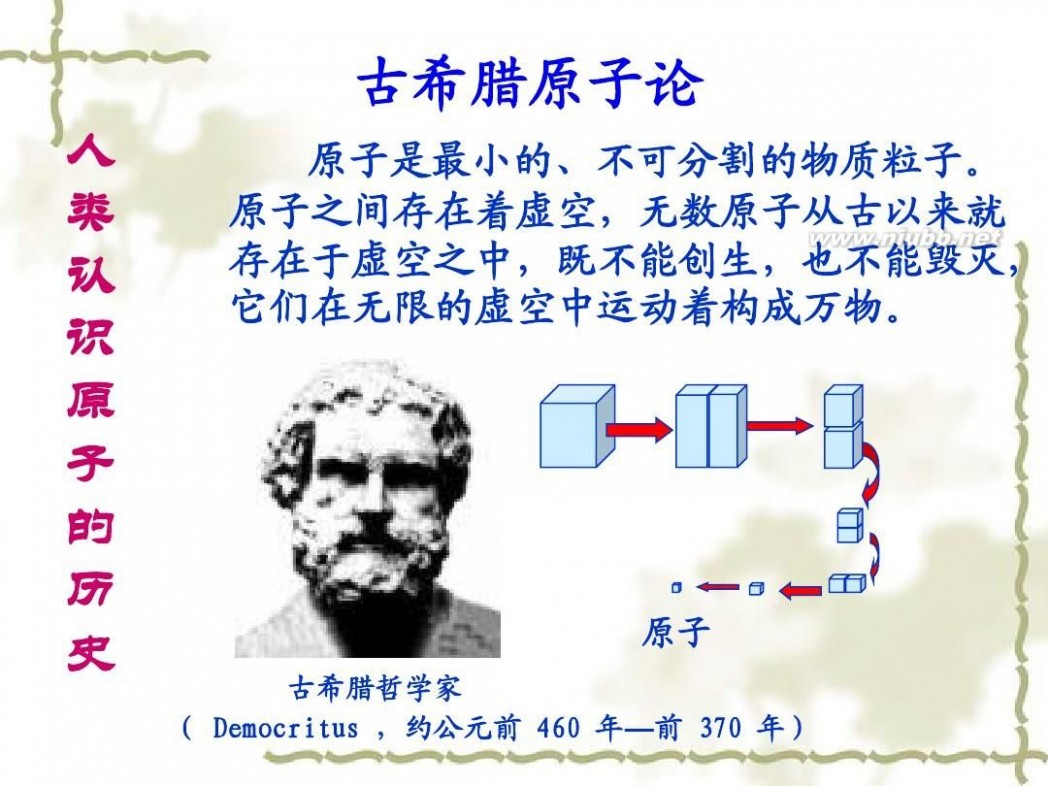
古希腊原子论
人 类 认 识 原 子 的 历 史
原子是最小的、不可分割的物质粒子。 原子之间存在着虚空,无数原子从古以来就 存在于虚空之中,既不能创生,也不能毁灭, 它们在无限的虚空中运动着构成万物。
原子
古希腊哲学家 ( Democritus ,约公元前 460 年—前 370 年)
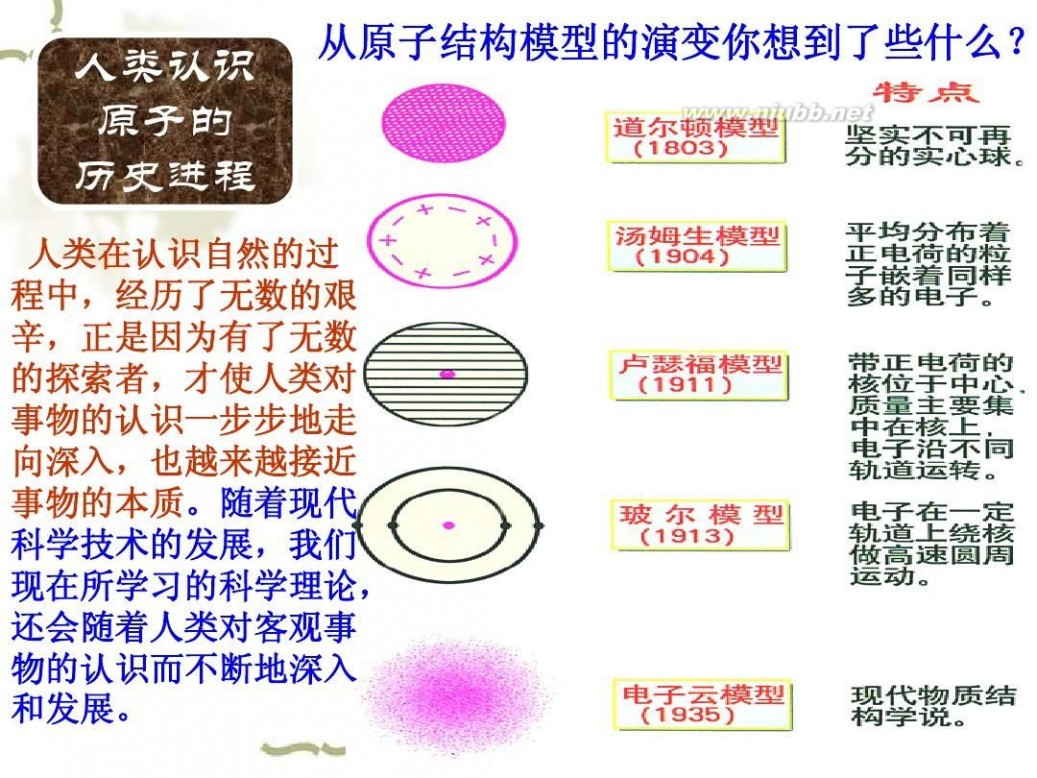
近代科学原子论(1803年) 道 尔 顿 原 子 模 型
?
?
一切物质都是由最小的 不能再分的粒子——原 子构成。 原子模型:原子是坚实 的、不可再分的实心球。
英国化学家道尔顿 (J.Dalton , 1766~1844)
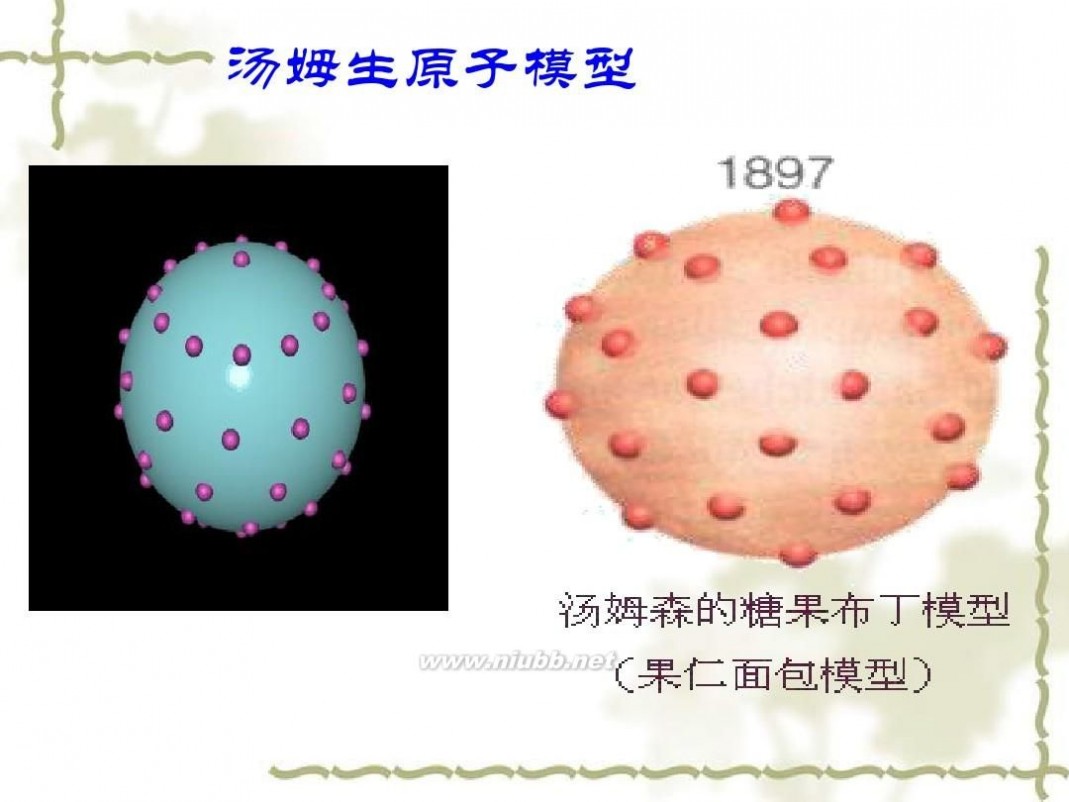
汤 姆 生 原 子 模 型
原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)
电子是种带负电、有一 定质量的微粒,普遍存 在于各种原子之中。 ? 汤姆生原子模型:原子 是一个平均分布着正电 荷的粒子,其中镶嵌着 许多电子,中和了电荷, 从而形成了中性原子。 原子是一个球体,正电 荷均匀分布在整个球体 英国物理学家汤姆生 内,电子像面包里的葡 (J.J.Thomson ,1856~1940) 萄干镶嵌其中。
?
汤姆生原子模型
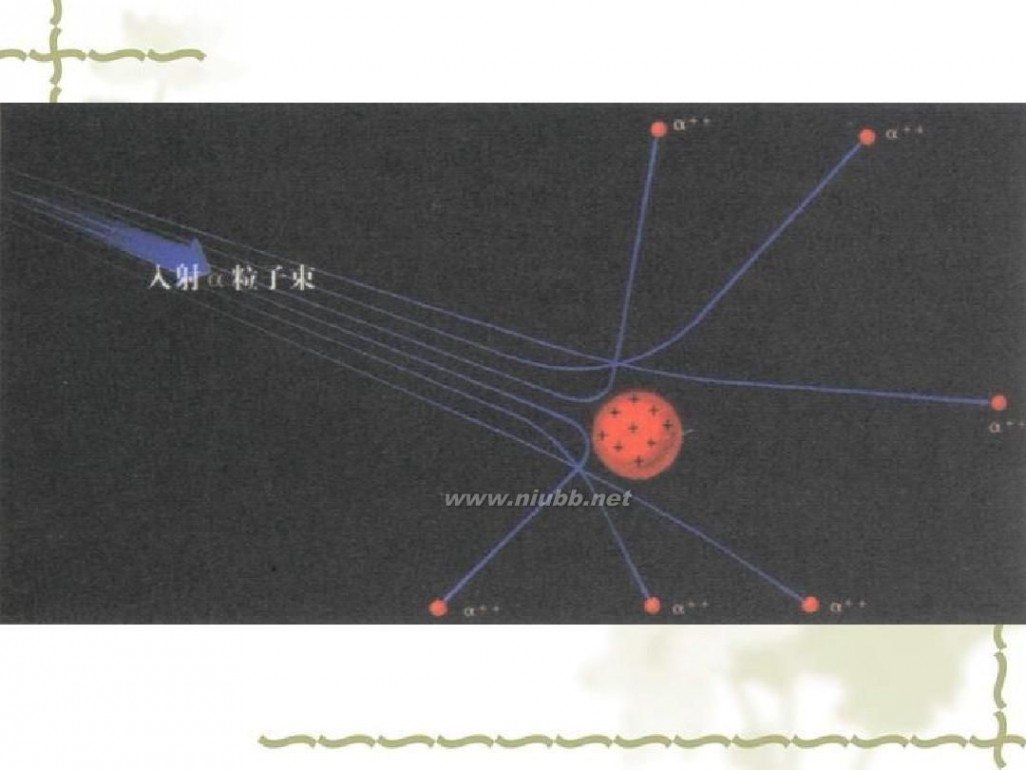
卢 瑟 福 原 子 模 型
α粒
子散射实验(1909年) ——原子有核
?
?
卢瑟福和他的助手做了 著名α粒子散射实验。根 据实验,卢瑟福在1911 年提出原子有核模型。 卢瑟福原子模型(又称 行星原子模型):原子 是由居于原子中心的带 正电的原子核和核外带 负电的电子构成。原子 核的质量几乎等于原子 的全部质量,电子在原 子核外空间绕核做高速 运动。
英国科学家卢瑟福 (E.Rutherford,1871~1937)
卢瑟福原子模型
玻尔原子模型(1913年)
玻 尔 原 子 模 型
?
?
?
玻尔借助诞生不久的量 子理论改进了卢瑟福的 模型。 玻尔原子模型(又称分 层模型):当原子只有 一个电子时,电子沿特 定球形轨道运转;当原 子有多个电子时,它们 将分布在多个球壳中绕 核运动。 不同的电子运转轨道是 具有一定级差的稳定轨 道。
丹麦物理学家玻尔 (N.Bohr,1885~1962)
玻尔原子模型
电 子 云 模 型
电子云模型 (现代物质结构学说)
?
?
现代科学家们在实验中发现,电子在原子核 周围有的区域出现的次数多,有的区域出现 的次数少,就像“云雾”笼罩在原子核周围。 因而提出了“电子云模型”。 电子云密度大的地方,表明电子在核外单位 体积内出现的机会多,反之,出现的机会少。 如:氢原子的电子云
现代物质结构学说
电子云
人类认识 原子的 历史进程
从原子结构模型的演变你想到了些什么?
人类在认识自然的过 程中,经历了无数的艰 辛,正是因为有了无数 的探索者,才使人类对 事物的认识一步步地走 向深入,也越来越接近 事物的本质。随着现代 科学技术的发展,我们 现在所学习的科学理论, 还会随着人类对客观事 物的认识而不断地深入 和发展。
【思考与交流】
原子的特点是什么? ? 原子是化学变化中的最小微粒 ? 原子的体积和质量都十分微小 ? 原子的大部分质量集中在原子核上
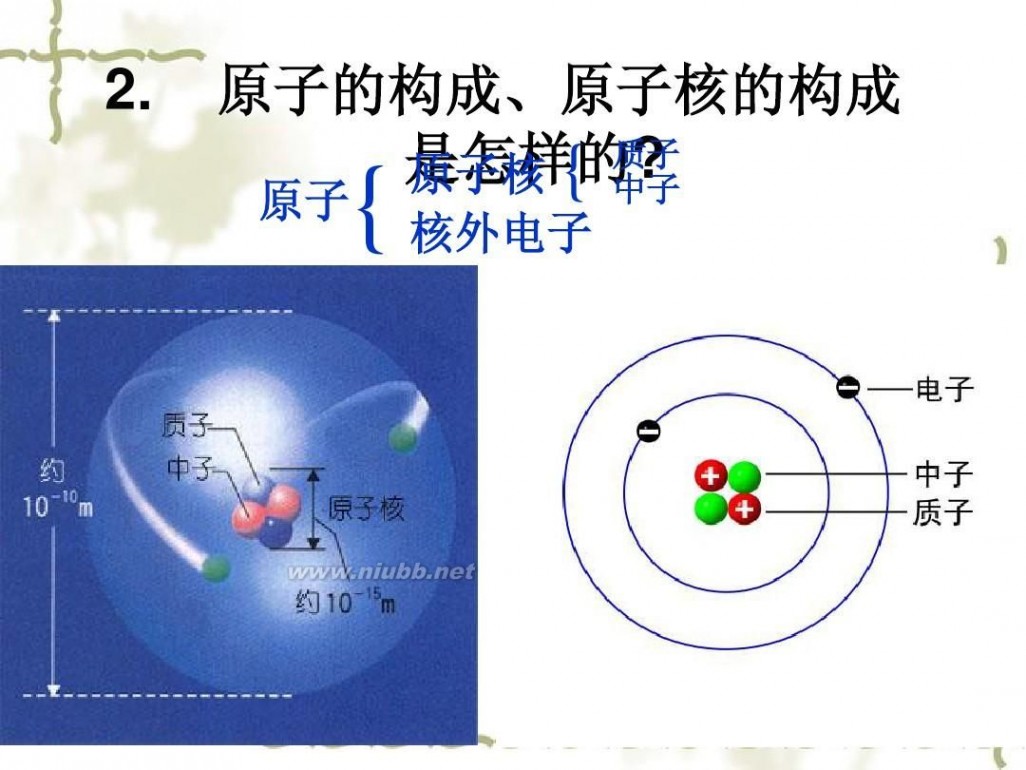
? 1.
2.
原子的构成、原子核的构成 质子 是怎样的? 原子核 { 中子
原子
{ 核外电子
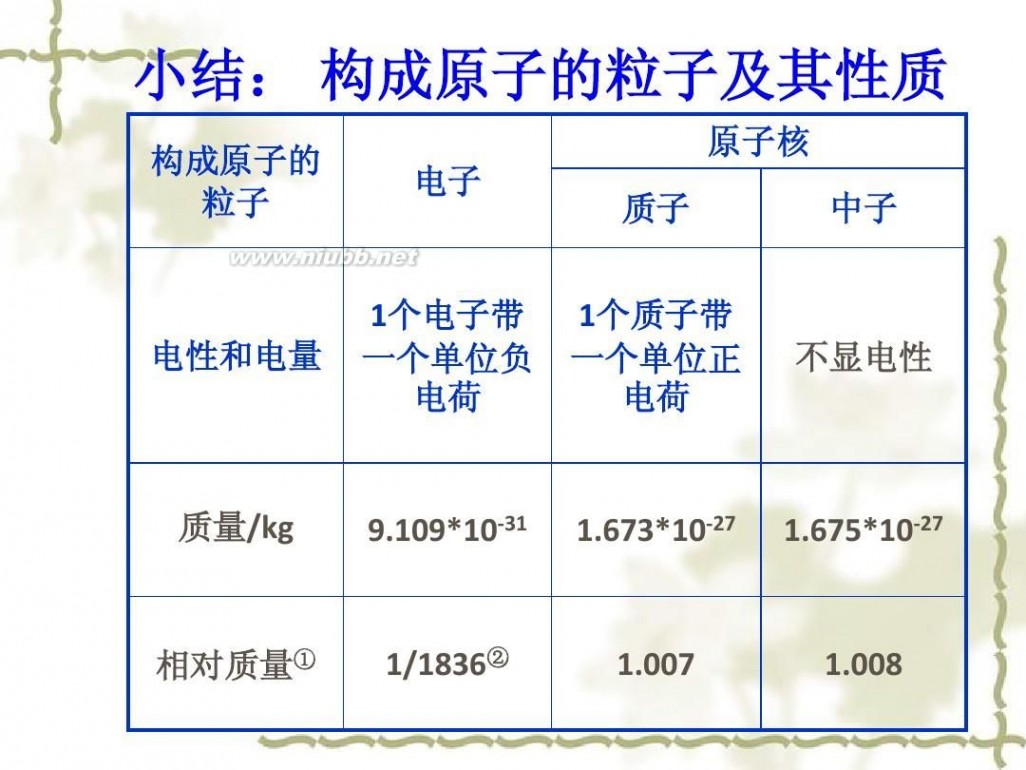
小结: 构成原子的粒子及其性质
构成原子的 粒子 原子核
电子
质子
中子
电性和电量
1个电子带 一个单位负 电荷
1个质子带 一个单位正 电荷
不显电性
质量/kg
9.109*10-31
1.673*10-27
1.675*10-27
相对质量①
1/1836②
1.007
1.008
【课堂达标测试1】
1、现代大爆炸理论认为:天然元素源于氢氦等发生的原 子核的融合反应。这于一百多年前,普鲁特运用思辨性推 测作出“氢是所有元素之母”的预言,恰好“一致”。下 列说法正确的是 ( ) C A科学研究中若能以思辨性推测为核心,就能加快科学的 进程 B普鲁特“既然氢最轻,它就是其他一切元素之母”的推 理是符合逻辑的 C“
一致”是巧合,普鲁特的预言没有科学事实和理论支 撑,只是一种猜测
D“现代大爆炸理论”是解释宇宙诞生的唯一正确的理论
2.支撑“宇宙大爆炸”理论的重要事实之一是
A.宇宙原子总数的88.6%是氢 B.地球上的元素绝大多数是金属 C.普鲁特“氢是元素之母”的预言 D.宇宙中存在少量稀有气体分子
( A
)
3.道尔顿的原子学说曾经起了很大的作用。他的学说中 主要有下列三个论点:①原子是不能再分的微粒;②同种 元素的原子的各种性质和质量都相同;③原子是微小的实 心球体。从现代原子——分子学说的观点看,你认为不正 确的是( D )
A
只有①
B
只有②
C
只有③
D
①②③
4.在1911年前后,新西兰出生的物理学家卢瑟福把一束 变速运动的α 粒子(质量数为4的带2个正电荷的质子粒)射 向一片极薄的金箔,他惊奇地发现,过去一直认为原子是 “实心球”,而这种“实心球”紧密排列而成的金箔,竟 为大多数α 粒子畅通无阻的通过,就像金箔不在那儿似的, 但也有极少数的。粒子发生偏转,或被笔直地弹回。根据 以上实验现象能得出关于金箔中Au原子结构的一些结论, 试写出其中的三点: 原子中存在原子核,它占原子中极小的体积 ①______________________________________________ 原子核带正电,且电荷数远远大于α 粒子 ②______________________________________________ 金的原子核质量远远大于α 粒子 ③______________________________________________
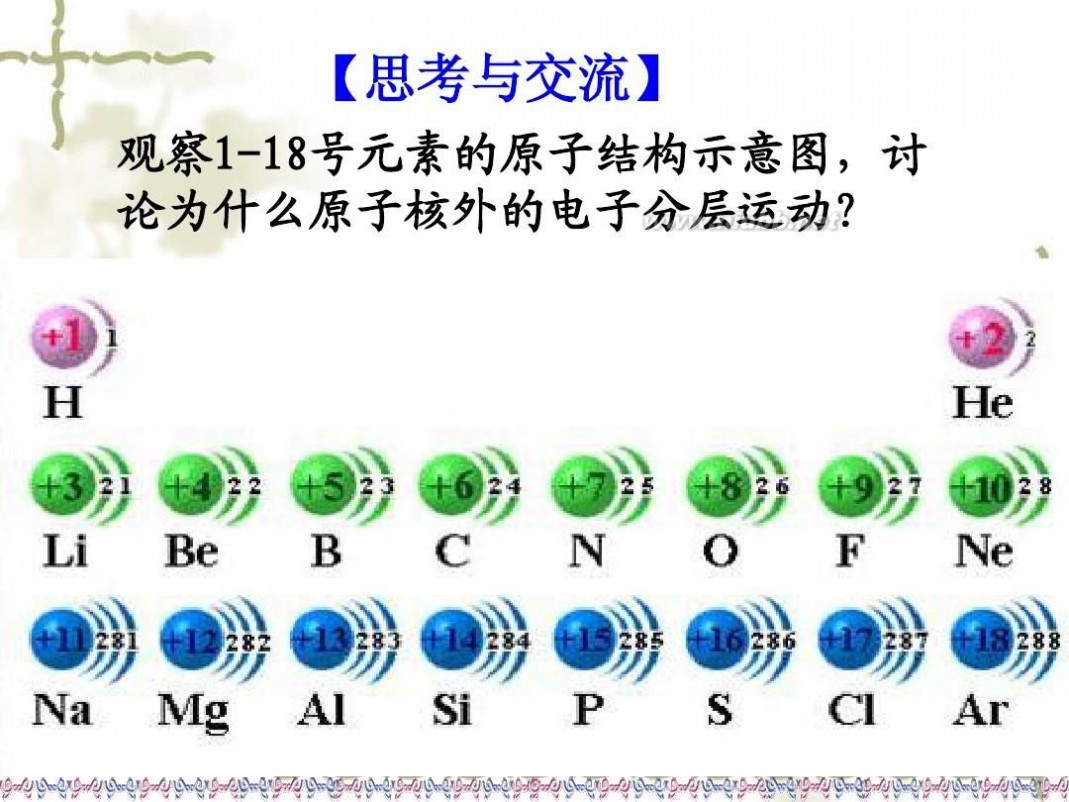
【思考与交流】
观察1-18号元素的原子结构示意图,讨 论为什么原子核外的电子分层运动?
核外电子分层排布
依据核外电子的能量不同: 离核远近:近 能量高低:低
1 K 2 L 3 M 4 N 5 O 6 P 7 Q
远 高
二、能层与能级 1.能层 (1)定义:在多电子的原子核外电子的能量是不同的, 按电子的能量差异,可以将核外电子分成不同的能层。
(2)表示方法及各能层所容纳的最多电子数:
【学与问】1、原子核外电子的每一个能层最多可容纳的 电子数与能层的序数(n)间存在什么关系?
每一个能层最多可容纳的电子数为2n2个。
2.能级 (1)定义:在多电子原子中,同一能层的电子,能量 可以不同,还可以把它们分成能级。
(2)表示方法及各能级所容纳的最多电子数:
【学与问】2.不同的能层分别有多少个能级,与能层的序 数(n)间存在什么关系? 任一能层的能级数等于该能层的序数。
【学与问】 3. 不同能层中,符号相同的能级中所容纳的 最多电子数是否相同?以s、p、d、f……排序的各能级 可容纳的最多电子数是多少? 不同能层中,符号相同的能级中所容纳的最多电子数 相同。以s、p、d、f……
排序的各能级可容纳的最多电 子数依次为1、3、5、7……的二倍,即2、6、10、14。
【课后探究】
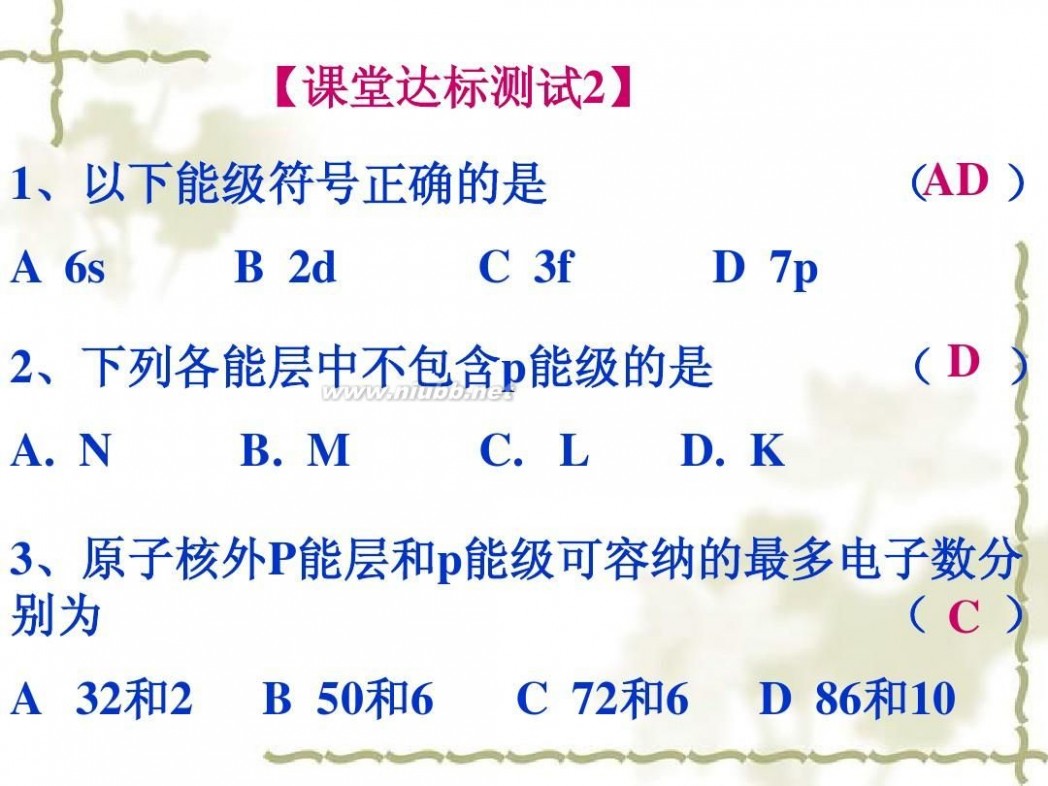
【课堂达标测试2】
1、以下能级符号正确的是
AD ) ( D 7p
A 6s
B 2d
C 3f
2、下列各能层中不包含p能级的是 A. N B. M C. L D. K
(D )
3、原子核外P能层和p能级可容纳的最多电子数分 别为 (C )
A 32和2 B 50和6 C 72和6 D 86和10
4.下列有关认识正确的是 (A ) A.各能级上最多的电子按s、p、d、f的顺序分 别为2、6、10、14 B.各能层的能级都是从s能级开始至f能级结束 C.各能层含有的能级数为n—1 D.各能层含有的电子数为2n2
5、下列各组微粒中,各能层电子数均达到2n2 个 的是 ( B) A.Ne和 Ar C.Ne和ClB.H-和Na+ D.F-和S2-
【课堂小结】
一.开天辟地—原子的诞生
二、能层与能级
作业: 1、完成本节作业纸 2、教材P5“构造原理”
第一节 原子结构
(第二课时)
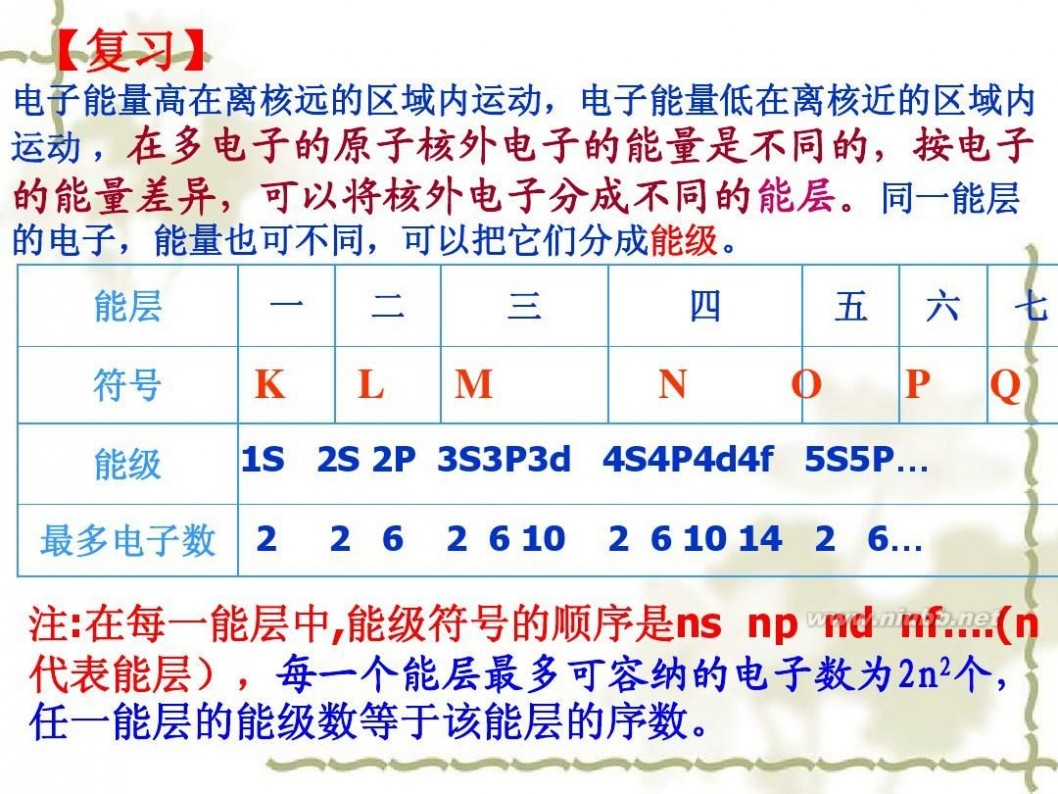
【复习】
电子能量高在离核远的区域内运动,电子能量低在离核近的区域内 运动 ,在多电子的原子核外电子的能量是不同的,按电子 的能量差异,可以将核外电子分成不同的能层。同一能层 的电子,能量也可不同,可以把它们分成能级。 能层 符号 能级 最多电子数 一 二 三 四 五 六 七
K
L
M
N
O
P
Q
1S 2S 2P 3S3P3d 4S4P4d4f 5S5P…
2
2 6
2 6 10
2 6 10 14 2 6…
注:在每一能层中,能级符号的顺序是ns np nd nf….(n 代表能层),每一个能层最多可容纳的电子数为2n2个, 任一能层的能级数等于该能层的序数。
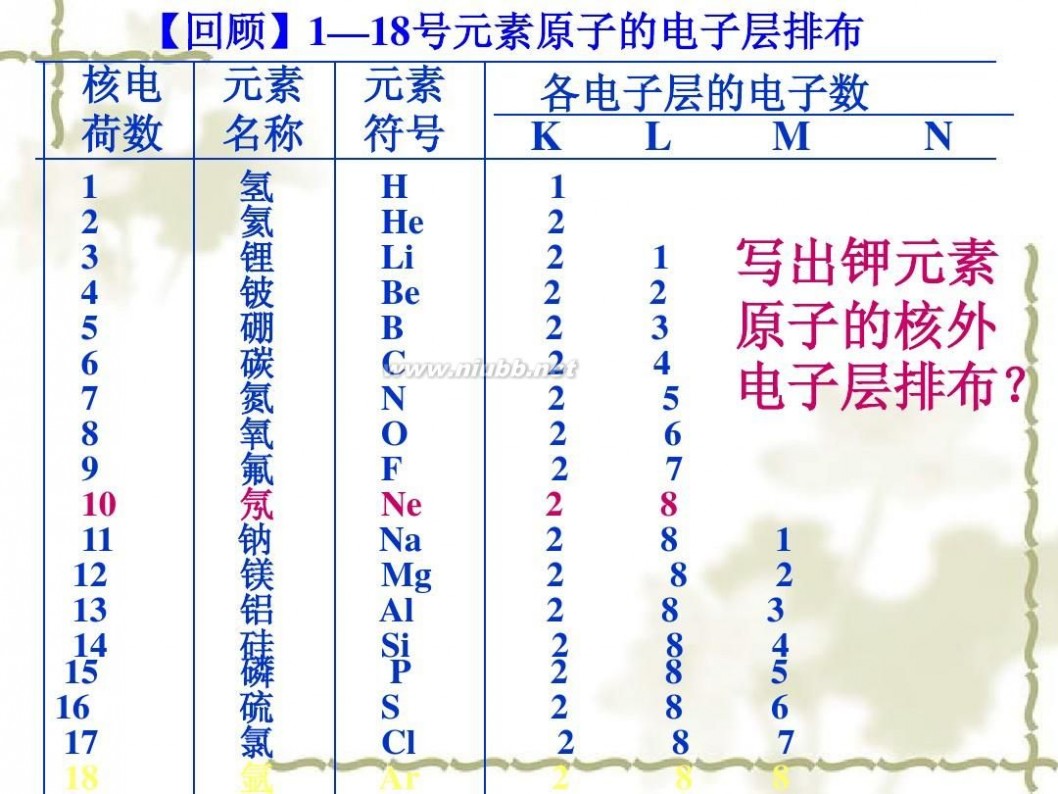
【回顾】1—18号元素原子的电子层排布
【回顾】1—18号元素原子的电子层排布 核电 元素 元素 各电子层的电子数 荷数 名称 符号 K L M
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 氢 氦 锂 铍 硼 碳 氮 氧 氟 氖 钠 镁 铝 硅 磷 硫 氯 氩 H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar 1 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 1 2 3 4 5 6 7 8 8 8 8 8 8 8 8 8
N
写出钾元素 原子的核外 电子层排布?
1 2 3 4 5 6 7 8
K元素原子的核外电子排布为什么 不是:2、8、9,而是2 、8、8、1呢?
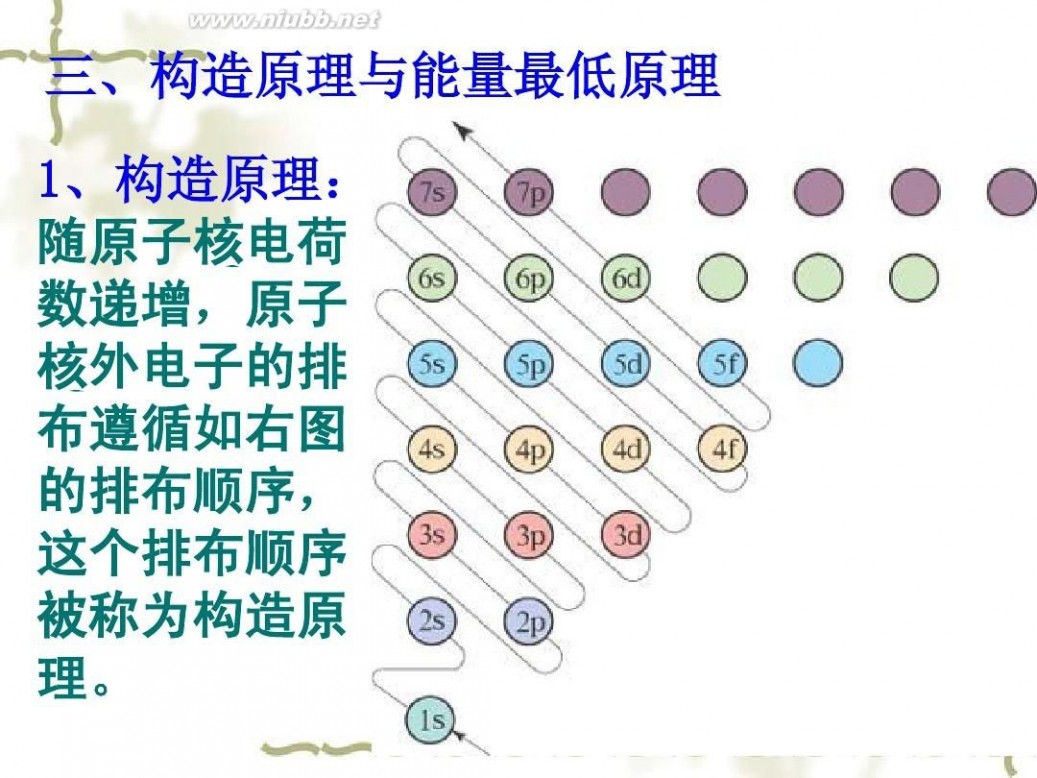
三、构造原理与能量最低原理
1、构造原理: 随原子核电荷 数递增,原子 核外电子的排 布遵循如右图 的排布顺序, 这个排布顺序 被称为构造原 理。
构造原理中排布顺序的实质
------各能级的能量高低顺序 1)相同能层的不同能级的能量高低顺序 : ns<np<nd<nf 2)英文字母相同的不同能级的能量高低顺序: 1s<2s<3s<4s;2p<3p<4p; 3d<4d 3) 不同层不同能级可由下面的公式得出: ns < (n-2)f < (n-1)d < np (n为能层序数)
2、构造原理的应用
(1)根据构造原理,电子所排的能级顺序为: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f … _______________________________________ (2)原子的电子排布式:用数字在能级符号
右上角表明该能级上的排布的电子数。 【练习】 氢 H
1s1
钠 Na 钾 K
1s22s22p63s1
1s22s22p63s23p64s1
(3)原子的简化电子排布: 钠 Na的简化电子排布: [Ne]3s1
上式方括号里的符号的意义是: 该元素前一个周期的惰性气体电子排布结构
【学生活动】 你能仿照钠的简化电子排布式写出第8号元素氧、第14号 元素硅和第26号元素铁的简化电子排布式吗?
O:[He]2s22p4 Si:[Ne]3s23p2 Fe:[Ar]3d64s2
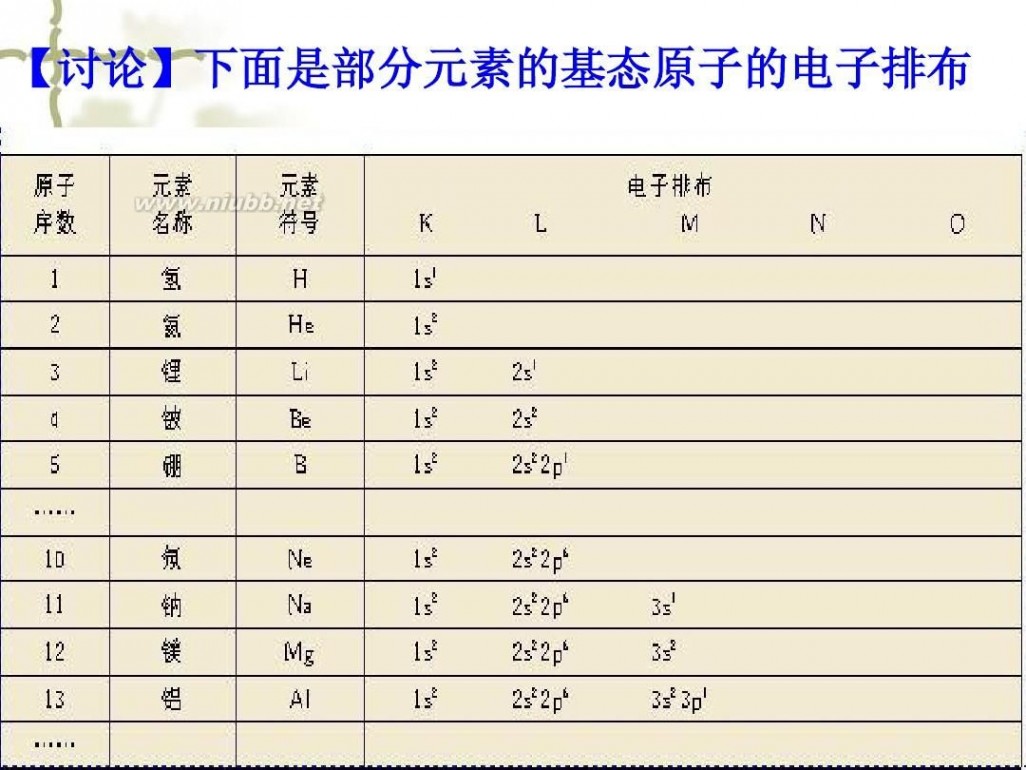
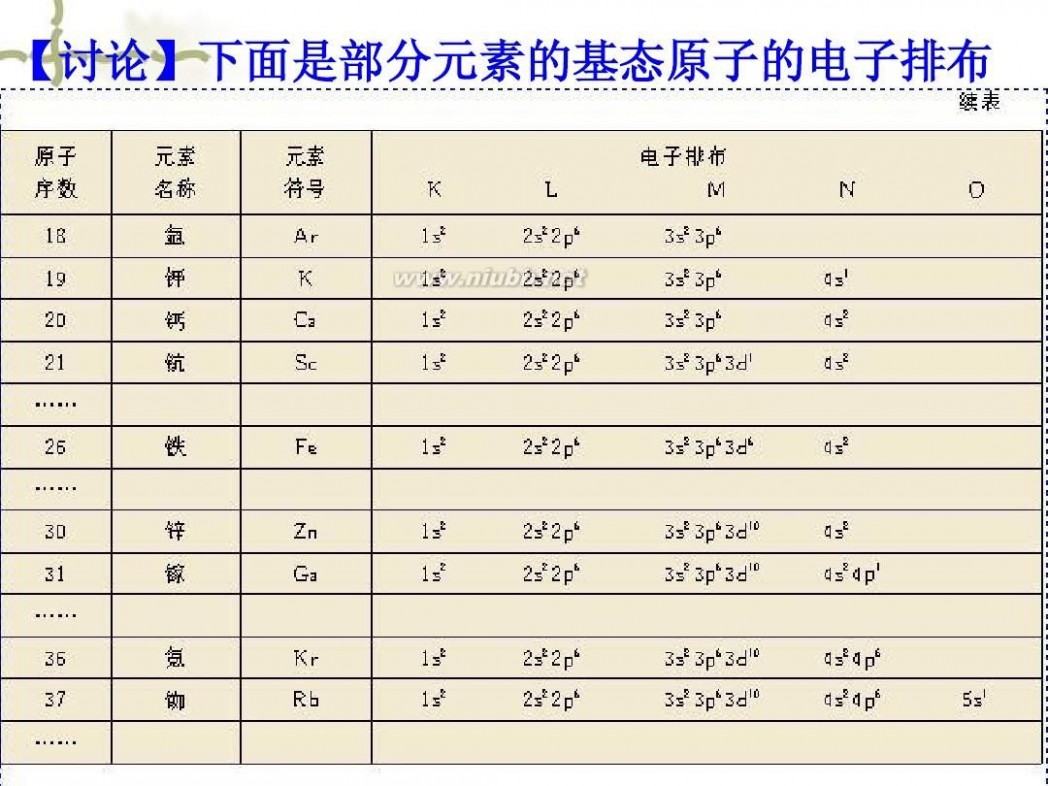
【讨论】下面是部分元素的基态原子的电子排布
【讨论】下面是部分元素的基态原子的电子排布
(4)原子核外电子排布规律
① 最外层最多只能容纳 8个电子(氦原子是2个); ② 次外层最多只能容纳18个电子; ③ 倒数第三层最多只能容纳32个电子; ④ 每个能层最多只能容纳2n2电子。 ⑤以s、p、d、f……排序的各能级可容纳的最多电子 数依次为1、3、5、7……的二倍,即2、6、10、14 ⑥核外电子总是尽量先排布在能量较低的能层,然 后由里向外,依次排布在能量逐步升高的能层。
【课后练习】 写出1~36号元素的原子核 外电子排布式和简化核外电 子排布式
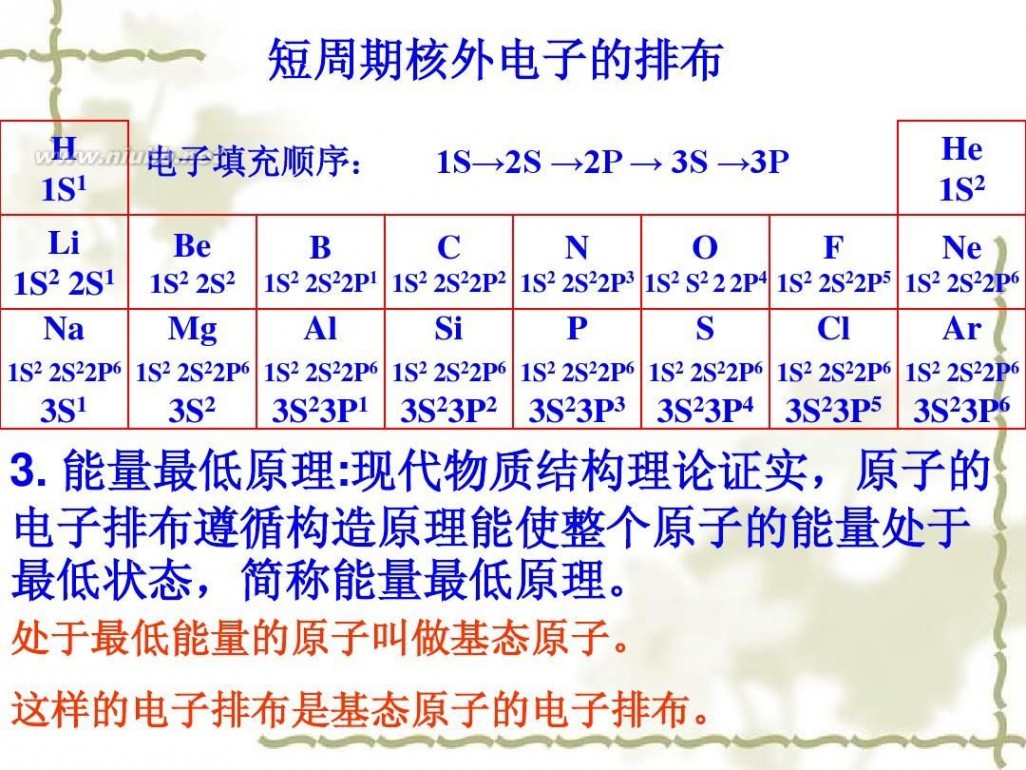
短周期核外电子的排布
H 1S1 电子填充顺序: B Al 1S→2S →2P → 3S →3P C Si N P O S F Cl He 1S2 Ne Ar
Li Be 1S2 2S1 1S2 2S2 Na Mg 3S1 3S2
1S2 2S22P1 1S2 2S22P2 1S2 2S22P3 1S2 S2 2 2P4 1S2 2S22P5 1S2 2S22P6
1S2 2S22P6 1S2 2S22P6 1S2 2S22P6 1S2 2S22P6 1S2 2S22P6 1S2 2S22P6 1S2 2S22P6 1S2 2S22P6
3S23P1 3S23P2 3S23P3 3S23P4 3S23P5 3S23P6
3. 能量最低原理:现代物质结构理论证实,原子的 电子排布遵循构造原理能使整个原子的能量处于 最低状态,简称能量最低原理。
处于最低能量的原子叫做基态原子。
这样的电子排布是基态原子的电子排布。
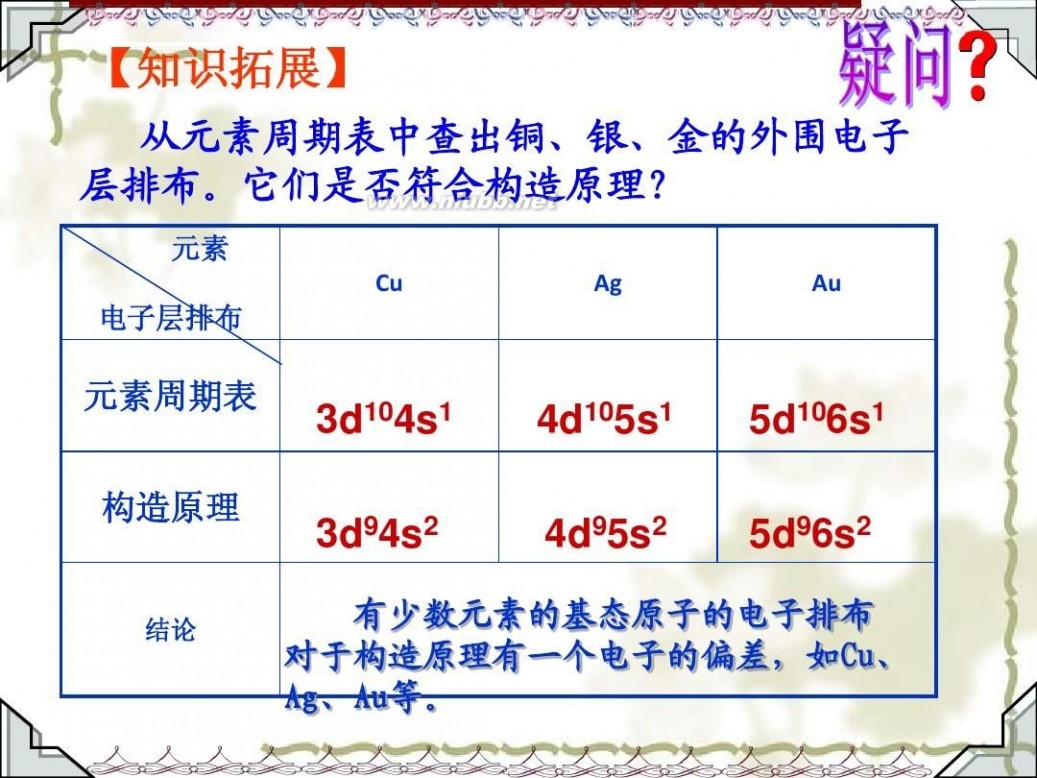
【知识拓展】
从元素周期表中查出铜、银、金的外围电子 层排布。它们是否符合构造原理?
元素
Cu Ag Au
电子层排布
元素周期表 构造原理
3d104s1 3d94s2
4d105s1 4d95s2
5d106s1 5d96s2
结论
有少数元素的基态原子的电子排布 对于构造原理有一个电子的偏差,如Cu、 Ag、Au等。
【课堂达标测试】
1.一个电子排布为1s22s22p63s23p1的元素最可 能的价态是( C ) A +1 B +2 C +3 D -1
2. 造原理揭示的电子排布能级顺序,实质是各能级能
量高低,若以E表示某能级的能量,下列能量大小顺序 中正确的是 A
A.E(3s)>E(2s)>E(1s)
C.E(4f)>E(4s)>E(3d)
B.E(3s)>E(3p)>E(3d)
D.E(5s)>E(4s)>E(4f)
3.下列各原子或离子的电子排布式错误的是( D )
A C Al Na+ 1s22s22p63s23p1 1s22s22p6 B D O2Si 1s22s22p6 1s22s22p2
4.下列表达方式错误的是( A B C D 甲烷的电子式 氟化钠的电子式 硫离子的核外电子排布式 碳-12原子
12 6C
D )
1s22s22p63s23p4
5、下列有几元素的核外电荷数,其中
最外层 电子数目最多的是( C ) A、8 B、14 C、18 D、20 6、由下列微粒的最外层电子排布,能确定形 成该微粒的元素在周期表中的位置的是( ) B A.1s2 C.2s22p6 B.3s23p1 D.ns2np3
小结:排步规律(一低四不超)
(1)能量最低原理 (2)各层最多容纳2n2 个电子
(3)最外层不超过8个(K层2个)
(4)次外层不超过18个,倒数第
三层不超过32个。
上述规律相互制约,相互联系
四、基态与激发态、光谱 1.基态原子与激发态原子 (1)基态原子:处于最低能 量的原子叫基态原子。 (2)激发态原子:当基态原 子的电子吸收能量后,电子 会跃迁到较高的能级,变成 激发态原子。 (3)基态与激发态的关系
吸收能量 基态原子 激发态原子
释放能量
2.原子光谱: 不同元素的原子发生跃迁时会吸收或释放不同的 光,可以用光谱仪摄取各种元素的电子的吸收光 谱或发射光谱,总称为原子光谱。
锂、氦、汞的发射光谱
锂、氦、汞的吸收光谱
3. 光谱分析: 在现代化学中,常利用原子光谱上的特征谱线来 鉴定元素,称为光谱分析。
4. 光谱分析的应用:
(1)通过原子光谱发现许多元素。
如:铯(1860年)和铷(1861年),其光谱中有特征 的篮光和红光。
又如:1868年科学家们通过太阳光谱的分析发现了稀 有气体氦。
(2)化学研究中利用光谱分析检测一些物质的 存在与含量等
【课堂达标测试2】
原子的电子排布遵循构造原理能使整个原子的 1________________________________________ 能量处于最低状态 ________________ ,简称能量最低原理。 _________________________叫做基态原子 处于最低能量的原子
1、当基态原子的电子吸收能量后 ,电子会 跃迁到较高能级 ______________,变成激发态原子。电子从较 高能量的激发态跃迁到较低能量的激发态乃至 基态时,将_________能量。光(辐射)是电 释放 子___________能量的重要形式之一。 释放
3、不同元素的原子发生跃迁时会吸收或释放 不同的光,可以用光谱仪摄取各种元素的电 吸收 发射 子的________光谱或__________光谱,总称 原子 _______光谱。许多元素是通过原子光谱发现 的。在现代化学中,常利用原子光谱上的特 光谱分析 征谱线来鉴定元素,称为________。
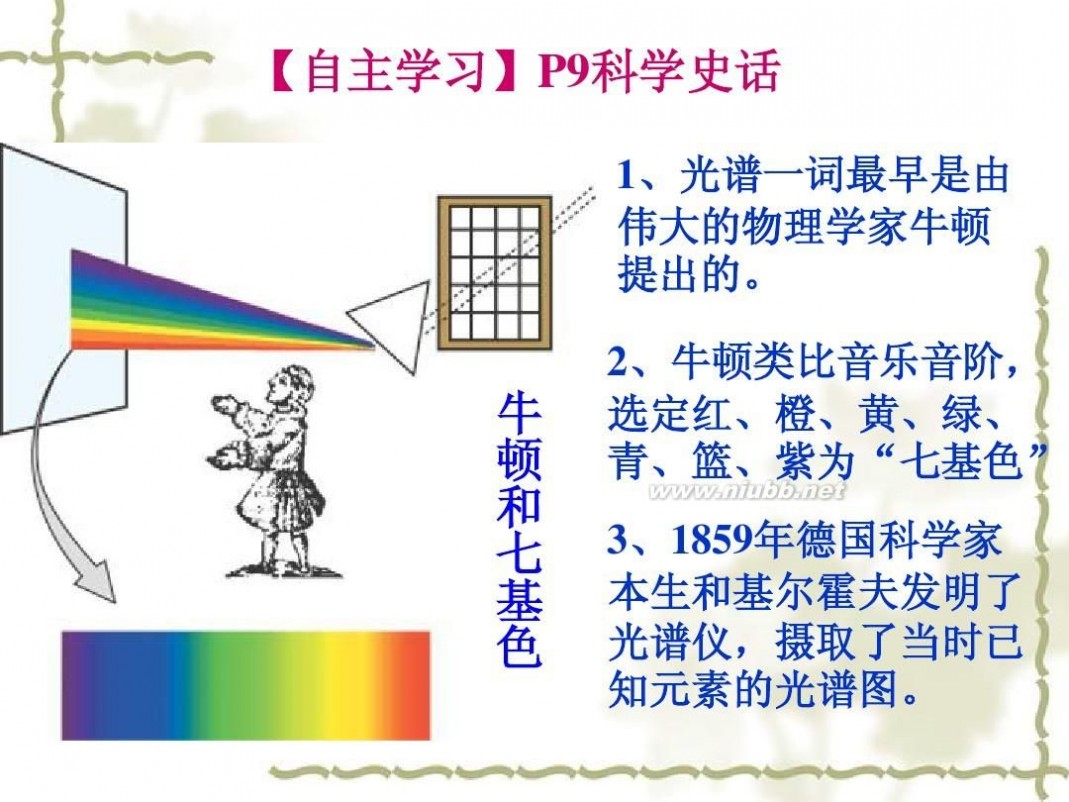
【自主学习】P9科学史话
1、光谱一词最早是由 伟大的物理学家牛顿 提出的。
牛 顿 和 七 基 色
2、牛顿类比音乐音阶, 选定红、橙、黄、绿、 青、篮、紫为“七基色”
3、1859年德国科学家 本生和基尔霍夫发明了 光谱仪,摄取了当时已 知元素的光谱图。
【课堂小结】
三、构造原理与能量最低原理
四、基态与激发态、光谱
作业: 1、完成本节作业纸 2、教材P10“
电子云与原子轨道”
二 : 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT
原子结构 原子结构》优秀课件PPT

原子结构 原子结构》优秀课件PPT

61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1