一 : 常温下氢氧化钾的溶解度曲线?常温下氢氧化钾(KOH)的溶解度曲线
常温下氢氧化钾的溶解度曲线?
常温下氢氧化钾(KOH)的溶解度曲线或者是该如何调出氢氧化钾饱和溶液
你用500gKOH溶于100g水,然后再倒出上清液就OK了
二 : I.如图1,根据氢氧化钙的溶解度曲线,完成下列问题:(1)曲线上满足A点所示溶液在温度升高会产生的现
| I.如图1,根据氢氧化钙的溶解度曲线,完成下列问题: (1)曲线上满足A点所示溶液在温度升高会产生的现象是______,此时的溶液中溶质质量分数将______(填“变大”、“变小”或“不变”). (2)若曲线上满足A点所示溶液中加入生石灰,此时溶液中溶质的质量分数将______(填“变大”、“变小”或“不变”). Ⅱ.如图2,根据氯化钠的溶解度曲线完成下列问题: 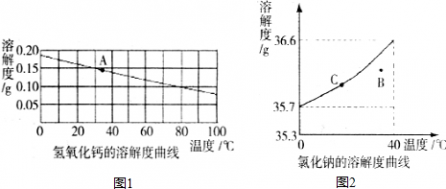 (3)B点所示溶液为对应温度下氯化钠的______(填“饱和溶液”或“不饱和溶液”). (4)将C点所示溶液升高温度至40℃(忽略水的蒸发),此时溶液中溶质的质量分数______(填“变大”、“变小”或“不变”). (5)C点可表示20℃时氯化钠的溶解度为36.0g,若将满足C所示的溶液恒温蒸发10g水,析出的氯化钠的质量为______. |
| Ⅰ、(1)氢氧化钙的溶解度随着温度的升高而减小,溶解度曲线上的点表示该温度下某物质的溶解度,故A点所示溶液是饱和溶液,升高温度,其溶解度减小,溶质析出,出现浑浊,溶质减少,溶剂不变,所以溶质的质量变小; 故答案为: 出现浑浊;变小; (2)生石灰溶于水放热,使溶液温度升高,氢氧化钙的溶解度变小,溶质析出,所以溶质的质量分数变小; 故答案为:变小; Ⅱ、(3)溶解度曲线上的点表示该温度下的饱和溶液,曲线下的点所示溶液表示该物质的不饱和溶液; 故答案为:不饱和溶液; (4)升高温度,氯化钠的溶解度升高,溶质质量不变,溶剂质量不变,则溶液的质量不变,根据溶质的质量分数=
故答案为:不变; (5)20℃时氯化钠的溶解度为36.0g,表示20℃时100g水中最多溶解36.0g氯化钠,恒温蒸发10g水,说明温度不变,则氯化钠的溶解度不变,10g水最多溶解3.6g氯化钠; 故答案为:3.6g. |
考点:
考点名称:饱和溶液,不饱和溶液饱和溶液和不饱和溶液的概念: 不饱和溶液
不饱和溶液 不饱和石灰水概念的理解:
不饱和石灰水概念的理解: 不饱和溶液(或不饱和溶液
不饱和溶液(或不饱和溶液 饱和溶液。不发生结晶的前提下)
饱和溶液。不发生结晶的前提下) 饱和溶液
饱和溶液 饱和溶液(不发生结晶的前提下)
饱和溶液(不发生结晶的前提下) 不饱和溶液
不饱和溶液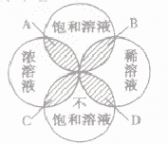 A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液 =
=
 ×100%
×100% 。
。 影响溶质质量分数的因素:
影响溶质质量分数的因素: ×100%
×100% | 方法 | 计算依据 | 计算公式 | |
| 溶液的稀释 | ①加水稀释 ②加稀溶液稀释 | ①加水稀释前后,溶液中溶质的质量不变 ②用稀溶液稀释浓溶液时。稀溶液中溶质的质量与浓溶液中溶质的质量之和等于混合后溶液中溶质的质量 | 加水稀释:稀释前后溶液中溶质的质量不变 m浓×ω浓%=(m浓+m水)×ω稀% |
| 溶液的浓缩 | ①添加溶质 ②蒸发溶剂 ③加入浓溶液 | ①原溶液中的溶质与后加入的溶质质量之和等于混合后溶液中的溶质质量 ②蒸发溶剂前后溶液中溶质的质量不变(没有溶质析出) ③原溶液中的溶质与后加入浓溶液中的溶质质量之和等于混合后溶液中的溶质质量 | 蒸发浓缩:浓缩前后溶液中溶质的质量不变(m稀-m水)×ω浓%=m稀×ω稀% |
 ×100g]可推导出:
×100g]可推导出: ,
,
| 溶解度 | 溶质质量分数 | |
| 意义 | 物质溶解性的量度,受外界温度的影响 | 表示溶液中溶质质量的多少,不受外界条件影响 |
| 容积要求 | 100g | 无要求 |
| 温度要求 | 与温度有关 | 一般与温度无关 |
| 溶液是否饱和 | 一定达到饱和 | 不一定饱和 |
| 计算公式 |  ×100g ×100g | 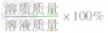 |
| 单位 | 克 | 无单位 |
| 联系 | 饱和溶液中溶质的质量分数= | |
 ×100%
×100% 。
。
61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1