一 : 硅孔雀石是一种含铜的矿石,含铜形态为,同时含有等杂质。以硅孔雀石为原料制取硫酸铜的工艺流程如下图:请
硅孔雀石是一种含铜的矿石,含铜形态为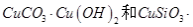 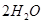 ,同时含有 ,同时含有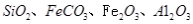 等杂质。以硅孔雀石为原料制取硫酸铜的工艺流程如下图: 等杂质。以硅孔雀石为原料制取硫酸铜的工艺流程如下图: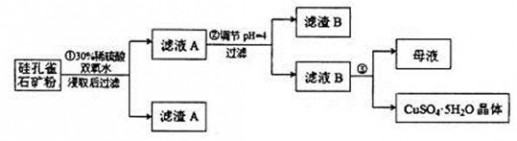 请回答下列问题: (1)完成步骤①中稀硫酸与 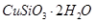 发生反应的化学方程式 发生反应的化学方程式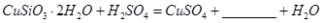 ; ;用离子方程式表示双氧水的作用_____________________________。 (2)步骤②调节溶液pH选用的最佳试剂是__________________
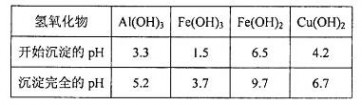 由上表可知:当溶液pH=4时,可以完全除去的离子是______,不能完全除去的离子是________。 (4)滤液B通过蒸发浓缩(设体积浓缩为原来的一半)、冷却结晶可以得到 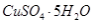 晶体。某同学认为上述操作会拌有硫酸铝晶体的析出。请你结合相关数据对该同学的观点予以评价(已知常温下, 晶体。某同学认为上述操作会拌有硫酸铝晶体的析出。请你结合相关数据对该同学的观点予以评价(已知常温下,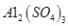 饱和溶液中 饱和溶液中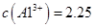 mol mol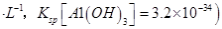 ______________。 ______________。(5)若要测定硫酸铜晶体中结晶水的含量,需要的仪器是酒精灯、托盘天平、三角架、泥三角、玻璃棒、干燥器、坩埚钳、研钵、药匙、_________________。实验过程中硫酸铜晶体加热失水后在空中冷却后称量,则测定结果______________(填“偏高”、 “偏低”或“不变”)。 |
(1)H4SiO4(1分) 2Fe2++H2O2+2H+= 2Fe3++2H2O(2分) (2)B(2分) (3)Fe3+(2分),Al3+(2分) (4)该同学的观点是错误的(1分)通过计算可知,滤液B中C(Al3+)=3.2×10-4mol?L-1,浓缩后C(Al3+)=6.4×10-4mol?L-1《2.25 mol?L-1,所以不会有硫酸铝晶体洗出。(2分) (5)坩埚(1分)偏低(1分) |
试题分析:(1)根据原子守恒可知缺H4SiO4,孔雀石酸溶后有Fe2+,双氧水有强氧化性,发生氧化还原反应: 2Fe2++H2O2+2H+= 2Fe3++2H2O;(2)调节pH=4的目的是沉淀Fe3+,最后得到硫酸铜晶体,为不引入杂质,选择B;(3)结合表中所给数据分析;(4)该同学的观点是错误的,通过计算可知,滤液B中C(Al3+)=3.2×10-4mol?L-1,浓缩后C(Al3+)=6.4×10-4mol?L-1《2.25 mol?L-1,所以不会有硫酸铝晶体洗出;(5)坩埚,硫酸铜在空气中中冷却后吸收了部分水,导致质量增大,测得结晶水含量偏低。 |
考点:
考点名称:离子方程式离子方程式: ”及状态符号“↑”和“↓”运用是否正确。
”及状态符号“↑”和“↓”运用是否正确。 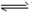 ”。复分解反应、水解反应生成的难溶物用“↓”,气体用“↑”;单水解反应生成的难溶物不用“↓”,气体不用“↑”。
”。复分解反应、水解反应生成的难溶物用“↓”,气体用“↑”;单水解反应生成的难溶物不用“↓”,气体不用“↑”。  ,正确为:
,正确为:
书写与量有关的离子方程式:
基本方法是:把物质的量少的物质的系数定为1,其他物质按最大量消耗。
1.因滴加顺序不同造成连续反应
HCl与Na2CO3向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3-(2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3- (2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
向AlCl3溶液中滴入NaOH溶液至过量,其离子反应分步写 (1)Al3++3OH-==Al(OH)3↓ (2)Al(OH)3+OH-==AlO2-+2H2O
若向NaOH溶液中加入少量AlCl3溶液,其离子反应一步完成 Al3++4OH-==AlO2-+2H2O
若向足量Al2(SO4)3溶液中加入少量的NaOH溶液,其离子方程式为: Al3++3OH-==Al(OH)3↓
向AgNO3溶液中滴入稀NH3·H2O至过量,其离子反应分步写(1) Ag++NH3·H2O==AgOH↓+NH4+(2)AgOH+2NH3·H2O==Ag(NH3)2++OH-+2H2O
若向NH3·H2O溶液中加入少量AgNO3,其离子反应一步完成 Ag++3NH3·H2O==Ag(NH3)2++OH-+NH4++2H2O
若向足量AgNO3溶液中滴入少量NH3·H2O,其离子方程式为:Ag++NH3·H2O==AgOH↓+NH4+
向NaOH溶液中通人CO2气体至过量,其离子反应分步写 (1)2OH-+CO2==CO32-+H2O (2)CO32-+CO2+H2O==2HCO3-
若向足量NaOH溶液中通人少量CO2气体,其离子方程式为: 2OH-+CO2==CO32-+H2O
若向NaOH溶液中通人过量CO2气体,其离子反应一步完成 OH-+CO2==HCO3-
2.过量型:
向足量的Ca(HCO3)2溶液中逐渐滴入NaOH溶液 OH-+Ca2++HCO3-==H2O+CaCO3↓
向足量的NaOH溶液中逐渐滴入Ca(HCO3)2溶液 Ca2++2HCO3-+2OH-==2H2O+CaCO3↓+CO32-
Fe与HNO3:铁过量时:Fe+4HNO3==Fe(NO3)3+NO↑+2H2O
铁不足时:3Fe+8HNO3==3Fe(NO3)2+2NO↑+4H2O
3.定量型:
因还原性I->Fe2+>Br-,所以在FeI2或者FeBr2中通入一定量的Cl2,发生不同的离子反应,依次为:
(1)2I-+Cl2==2Cl-+I2(2)2Fe2++Cl2==2Fe3++2Cl-(3)2Br-+Cl2==2Cl-+Br2
4.目标型
向明矾溶液逐滴滴加Ba(OH)2溶液至硫酸根离子刚好沉淀完全 Al3++SO42-+Ba2++4OH-==AlO2-+2BaSO4↓+2H2O
向明矾溶液逐滴滴加Ba(OH)2溶液至铝离子刚好沉淀完全 Al3+SO42-+Ba2++3OH-==Al(OH)3↓+2BaSO4↓

二 : 脱硫:脱硫-工艺种类,脱硫-方程
脱硫一般分为烟气脱硫和橡胶专业的脱硫,烟气脱硫指除去烟气中的硫及化合物的过程,主要指烟气中的SO、SO2,以达到环境要求。 橡胶专业的脱硫(devulcanizing)指采用不同加热方式并应用相应设备使废胶粉在再生剂参与下与硫键断裂获得具有类似生胶性能的化学物理降解过程。
脱硫技术_脱硫 -工艺种类
石膏法
 湿法脱硫工艺流程图
湿法脱硫工艺流程图石灰石——石膏法脱硫工艺是世界上应用最广泛的1种脱硫技
术,日本、德国、美国的火力发电厂采用的烟气脱硫装置约90%采用此工艺。
它的工作原理是:将石灰石粉加水制成浆液作为吸收剂泵入吸收塔与烟气充分接触混合,烟气中的二氧化硫与浆液中的碳酸钙以及从塔下部鼓入的空气进行氧化反应生成硫酸钙,硫酸钙达到一定饱和度后,结晶形成二水石膏。经吸收塔排出的石膏浆液经浓缩、脱水,使其含水量小于10%,然后用输送机送至石膏贮仓堆放,脱硫后的烟气经过除雾器除去雾滴,再经过换热器加热升温后,由烟囱排入大气。由于吸收塔内吸收剂浆液通过循环泵反复循环与烟气接触,吸收剂利用率很高,钙硫比较低,脱硫效率可大于95%。
系统组成:
(1)石灰石储运系统
(2)石灰石浆液制备及供给系统
(3)烟气系统
(4)SO2 吸收系统
(5)石膏脱水系统
(6)石膏储运系统
(7)浆液排放系统
(8)工艺水系统
(9)压缩空气系统
(10)废水处理系统
(11)氧化空气系统
(12)电控制系统
技术特点:
⑴、吸收剂适用范围广:在FGD装置中可采用各种吸收剂,包括石灰石、石灰、镁石、废苏打溶液等;
⑵、燃料适用范围广:适用于燃烧煤、重油、奥里油,以及石油焦等燃料的锅炉的尾气处理;
⑶、燃料含硫变化范围适应性强:可以处理燃料含硫量高达8%的烟气;
⑷、机组负荷变化适应性强:可以满足机组在15~100%负荷变化范围内的稳定运行;
⑸、脱硫效率高:一般大于95%,最高达到98%;
⑹、专利托盘技术:有效降低液/气比,有利于塔内气流均布,节省物耗及能耗,方便吸收塔内件检修;
⑺、吸收剂利用率高:钙硫比低至1.02~1.03;
⑻、副产品纯度高:可生产纯度达95%以上的商品级石膏;
⑼、燃煤锅炉烟气的除尘效率高:达到80%~90%;
⑽、交叉喷淋管布置技术:有利于降低吸收塔高度。
推荐的适用范围:
⑴、200MW及以上的中大型新建或改造机组;
⑵、燃煤含硫量在0.5~5%及以上;
⑶、要求的脱硫效率在95%以上;
⑷、石灰石较丰富且石膏综合利用较广泛的地区
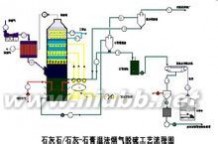
喷雾干燥法
 半干法脱硫工艺流程
半干法脱硫工艺流程喷雾干燥法脱硫工艺以石灰为脱硫吸收剂,石灰经消化并加水制成消石灰乳,消
石灰乳由泵打入位于吸收塔内的雾化装置,在吸收塔内,被雾化成细小液滴的吸收剂与烟气混合接触,与烟气中的SO2发生化学反应生成CaSO3,烟气中的SO2被脱除。与此同时,吸收剂带入的水分迅速被蒸发而干燥,烟气温度随之降低。脱硫反应产物及未被利用的吸收剂以干燥的颗粒物形式随烟气带出吸收塔,进入除尘器被收集下来。脱硫后的烟气经除尘器除尘后排放。为了提高脱硫吸收剂的利用率,一般将部分除尘器收集物加入制浆系统进行循环利用。该工艺有2种不同的雾化形式可供选择,1种为旋转喷雾轮雾化,另1种为气液两相流。
喷雾干燥法脱硫工艺具有技术成熟、工艺流程较为简单、系统可靠性高等特点,脱硫率可达到85%以上。该工艺在美国及西欧一些国家有一定应用范围(8%)。脱硫灰渣可用作制砖、筑路,但多为抛弃至灰场或回填废旧矿坑。
磷铵肥法
 脱硫流程
脱硫流程磷铵肥法烟气脱硫技术属于回收法,以其副产品为磷铵而命名。该工艺
过程主要由吸附(活性炭脱硫制酸)、萃取(稀硫酸分解磷矿萃取磷酸)、中和(磷铵中和液制备)、吸收(磷铵液脱硫制肥)、氧化(亚硫酸铵氧化)、浓缩干燥(固体肥料制备)等单元组成。它分为2个系统:
烟气脱硫系统——烟气经高效除尘器后使含尘量小于200mg/Nm3,用风机将烟压升高到7000Pa,先经文氏管喷水降温调湿,然后进入四塔并列的活性炭脱硫塔组(其中一只塔周期性切换再生),控制一级脱硫率大于或等于70%,并制得30%左右浓度的硫酸,一级脱硫后的烟气进入二级脱硫塔用磷铵浆液洗涤脱硫,净化后的烟气经分离雾沫后排放。
肥料制备系统——在常规单槽多浆萃取槽中,同一级脱硫制得的稀硫酸分解磷矿粉(P2O5 含量大于26%),过滤后获得稀磷酸(其浓度大于10%),加氨中和后制得磷氨,作为二级脱硫剂,二级脱硫后的料浆经浓缩干燥制成磷铵复合肥料。
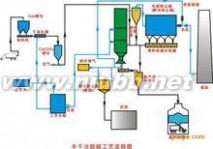
炉内喷钙尾部增湿法
 烟气脱硫工艺流程
烟气脱硫工艺流程炉内喷钙加尾部烟气增湿活化脱硫工艺是在炉内喷钙脱硫工艺的基础上在锅炉尾部增设了增湿段,以提高脱硫效率。该工艺多以石灰石粉为吸收剂,石灰石粉由气力喷入炉膛850~1150℃
温度区,石灰石受热分解为氧化钙和二氧化碳,氧化钙与烟气中的二氧化硫反应生成亚硫酸钙。由于反应在气固两相之间进行,受到传质过程的影响,反应速度较慢,吸收剂利用率较低。在尾部增湿活化反应器内,增湿水以雾状喷入,与未反应的氧化钙接触生成氢氧化钙进而与烟气中的二氧化硫反应。当钙硫比控制在2.0~2.5时,系统脱硫率可达到65~80%。由于增湿水的加入使烟气温度下降,一般控制出口烟气温度高于露点温度10~15℃,增湿水由于烟温加热被迅速蒸发,未反应的吸收剂、反应产物呈干燥态随烟气排出,被除尘器收集下来。
该脱硫工艺在芬兰、美国、加拿大、法国等国家得到应用,采用这一脱硫技术的最大单机容量已达30万千瓦。
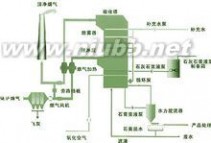
烟气循环流化床法
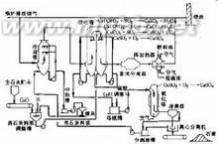 石灰 石膏法脱硫工艺流程
石灰 石膏法脱硫工艺流程烟气循环流化床脱硫工艺由吸收剂制备、吸收塔、脱硫灰再循环、除尘
器及控制系统等部分组成。该工艺一般采用干态的消石灰粉作为吸收剂,也可采用其它对二氧化硫有吸收反应能力的干粉或浆液作为吸收剂。
由锅炉排出的未经处理的烟气从吸收塔(即流化床)底部进入。吸收塔底部为1个文丘里装置,烟气流经文丘里管后速度加快,并在此与很细的吸收剂粉末互相混合,颗粒之间、气体与颗粒之间剧烈摩擦,形成流化床,在喷入均匀水雾降低烟温的条件下,吸收剂与烟气中的二氧化硫反应生成CaSO3 和CaSO4。脱硫后携带大量固体颗粒的烟气从吸收塔顶部排出,进入再循环除尘器,被分离出来的颗粒经中间灰仓返回吸收塔,由于固体颗粒反复循环达百次之多,故吸收剂利用率较高。
此工艺所产生的副产物呈干粉状,其化学成分与喷雾干燥法脱硫工艺类似,主要由飞灰、CaSO3、CaSO4和未反应完的吸收剂Ca(OH)2等组成,适合作废矿井回填、道路基础等。
典型的烟气循环流化床脱硫工艺,当燃煤含硫量为2%左右,钙硫比不大于1.3时,脱硫率可达90%以上,排烟温度约70℃。此工艺在国外目前应用在10~20万千瓦等级机组。由于其占地面积少,投资较省,尤其适合于老机组烟气脱硫。
海水脱硫
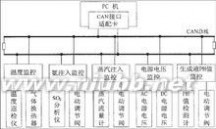 CAN等离子体烟气脱硫工艺
CAN等离子体烟气脱硫工艺海水脱硫工艺是利用海水的碱度达到脱除烟气中二氧化硫的1种脱硫方法
。在脱硫吸收塔内,大量海水喷淋洗涤进入吸收塔内的燃煤烟气,烟气中的二氧化硫被海水吸收而除去,净化后的烟气经除雾器除雾、经烟气换热器加热后排放。吸收二氧化硫后的海水与大量未脱硫的海水混合后,经曝气池曝气处理,使其中的SO32-被氧化成为稳定的SO42-,并使海水的PH值与COD调整达到排放标准后排放大海。海水脱硫工艺一般适用于靠海边、扩散条件较好、用海水作为冷却水、燃用低硫煤的电厂。海水脱硫工艺在挪威比较广泛用于炼铝厂、炼油厂等工业炉窑的烟气脱硫,先后有20多套脱硫装置投入运行。近几年,海水脱硫工艺在电厂的应用取得了较快的进展。此种工艺最大问题是烟气脱硫后可能产生的重金属沉积和对海洋环境的影响需要长时间的观察才能得出结论,因此在环境质量比较敏感和环保要求较高的区域需慎重考虑。
电子束法
 脱硫设备
脱硫设备该工艺流程有排烟预除尘、烟气冷却、氨的充入、电子束照射和副产品捕
集等工序所组成。锅炉所排出的烟气,经过除尘器的粗滤处理之后进入冷却塔,在冷却塔内喷射冷却水,将烟气冷却到适合于脱硫、脱硝处理的温度(约70℃)。烟气的露点通常约为50℃,被喷射呈雾状的冷却水在冷却塔内完全得到蒸发,因此,不产生废水。通过冷却塔后的烟气流进反应器,在反应器进口处将一定的氨水、压缩空气和软水混合喷入,加入氨的量取决于SOx浓度和NOx浓度,经过电子束照射后,SOx和NOx在自由基作用下生成中间生成物硫酸(H2SO4)和硝酸(HNO3)。然后硫酸和硝酸与共存的氨进行中和反应,生成粉状微粒(硫酸氨(NH4)2SO4与硝酸氨NH4NO3的混合粉体)。这些粉状微粒一部分沉淀到反应器底部,通过输送机排出,其余被副产品除尘器所分离和捕集,经过造粒处理后被送到副产品仓库储藏。净化后的烟气经脱硫风机由烟囱向大气排放。
氨水洗涤法
 烟气脱硫设备
烟气脱硫设备该脱硫工艺以氨水为吸收剂,副产硫酸铵化肥。锅炉排出的烟气经烟气换
热器冷却至90~100℃,进入预洗涤器经洗涤后除去HCI和HF,洗涤后的烟气经过液滴分离器除去水滴进入前置洗涤器中。在前置洗涤器中,氨水自塔顶喷淋洗涤烟气,烟气中的SO2被洗涤吸收除去,经洗涤的烟气排出后经液滴分离器除去携带的水滴,进入脱硫洗涤器。在该洗涤器中烟气进1步被洗涤,经洗涤塔顶的除雾器除去雾滴,进入脱硫洗涤器。再经烟气换热器加热后经烟囱排放。洗涤工艺中产生的浓度约30%的硫酸铵溶液排出洗涤塔,可以送到化肥厂进1步处理或直接作为液体氮肥出售,也可以把这种溶液进1步浓缩蒸发干燥加工成颗粒、晶体或块状化肥出售。
燃烧前脱硫法
燃烧前脱硫就是在煤燃烧前把煤中的硫分脱除掉,燃烧前脱硫技术主要有物理洗选煤法、化学洗选煤法、添加固硫剂、煤的气化和液化、水煤浆技术等。洗选煤是采用物理、化学或生物方式对锅炉使用的原煤进行清洗,将煤中的硫部分除掉,使煤得以净化并生产出不同质量、规格的产品。微生物脱硫技术从本质上讲也是1种化学法,它是把煤粉悬浮在含细菌的气泡液中,细菌产生的酶能促进硫氧化成硫酸盐,从而达到脱硫的目的;微生物脱硫技术目前常用的脱硫细菌有:属硫杆菌的氧化亚铁硫杆菌、氧化硫杆菌、古细菌、热硫化叶菌等。添加固硫剂是指在煤中添加具有固硫作用的物质,并将其制成各种规格的型煤,在燃烧过程中,煤中的含硫化合物与固硫剂反应生成硫酸盐等物质而留在渣中,不会形成SO2。煤的气化,是指用水蒸汽、氧气或空气作氧化剂,在高温下与煤发生化学反应,生成H2、CO、CH4等可燃混合气体(称作煤气)的过程。煤炭液化是将煤转化为清洁的液体燃料(汽油、柴油、航空煤油等)或化工原料的1种先进的洁净煤技术。水煤浆(Coal Water Mixture,简称CWM)是将灰份小于10%,硫份小于0.5%、挥发份高的原料煤,研磨成250~300μm的细煤粉,按65%~70%的煤、30%~35%的水和约1%的添加剂的比例配制而成,水煤浆可以像燃料油一样运输、储存和燃烧,燃烧时水煤浆从喷嘴高速喷出,雾化成50~70μm的雾滴,在预热到600~700℃的炉膛内迅速蒸发,并拌有微爆,煤中挥发分析出而着火,其着火温度比干煤粉还低。
燃烧前脱硫技术中物理洗选煤技术已成熟,应用最广泛、最经济,但只能脱无机硫;生物、化学法脱硫不仅能脱无机硫,也能脱除有机硫,但生产成本昂贵,距工业应用尚有较大距离;煤的气化和液化还有待于进1步研究完善;微生物脱硫技术正在开发;水煤浆是1种新型低污染代油燃料,它既保持了煤炭原有的物理特性,又具有石油一样的流动性和稳定性,被称为液态煤炭产品,市场潜力巨大,目前已具备商业化条件。
煤的燃烧前的脱硫技术尽管还存在着种种问题,但其优点是能同时除去灰分,减轻运输量,减轻锅炉的沾污和磨损,减少电厂灰渣处理量,还可回收部分硫资源。
炉内脱硫
炉内脱硫是在燃烧过程中,向炉内加入固硫剂如CaCO3等,使煤中硫分转化成硫酸盐,随炉渣排除。其基本原理是:
CaCO3==高温==CaO+CO2↑
CaO+SO2====CaSO3
2CaSO3+O2====2CaSO4
⑴LIMB炉内喷钙技术
早在本世纪60年代末70年代初,炉内喷固硫剂脱硫技术的研究工作已开展,但由于脱硫效率低于10%~30%,既不能与湿法FGD相比,也难以满足高达90%的脱除率要求。一度被冷落。但在1981年美国国家环保局EPA研究了炉内喷钙多段燃烧降低氮氧化物的脱硫技术,简称LIMB,并取得了一些经验。Ca/S在2以上时,用石灰石或消石灰作吸收剂,脱硫率分别可达40%和60%。对燃用中、低含硫量的煤的脱硫来说,只要能满足环保要求,不一定非要求用投资费用很高的烟气脱硫技术。炉内喷钙脱硫工艺简单,投资费用低,特别适用于老厂的改造。
⑵LIFAC烟气脱硫工艺
LIFAC工艺即在燃煤锅炉内适当温度区喷射石灰石粉,并在锅炉空气预热器后增设活化反应器,用以脱除烟气中的SO2。芬兰Tampella和ⅣO公司开发的这种脱硫工艺,于1986年首先投入商业运行。LIFAC工艺的脱硫效率一般为60%~85%。
加拿大最先进的燃煤电厂Shand电站采用LIFAC烟气脱硫工艺,八个月的运行结果表明,其脱硫工艺性能良好,脱硫率和设备可用率都达到了一些成熟的SO2控制技术相当的水平。中国下关电厂引进LIFAC脱硫工艺,其工艺投资少、占地面积小、没有废水排放,有利于老电厂改造。
烟气脱硫
简单介绍
(Flue gas desulfurization,简称FGD)
燃煤的烟气脱硫技术是当前应用最广、效率最高的脱硫技术。对燃煤电厂而言,在今后1个相当长的时期内,FGD将是控制SO2排放的主要方法。目前国内外火电厂烟气脱硫技术的主要发展趋势为:脱硫效率高、装机容量大、技术水平先进、投资省、占地少、运行费用低、自动化程度高、可靠性好等。
干式脱硫
该工艺用于电厂烟气脱硫始于80年代初,与常规的湿式洗涤工艺相比有以下优点:投资费用较低;脱硫产物呈干态,并和飞灰相混;无需装设除雾器及再热器;设备不易腐蚀,不易发生结垢及堵塞。其缺点是:吸收剂的利用率低于湿式烟气脱硫工艺;用于高硫煤时经济性差;飞灰与脱硫产物相混可能影响综合利用;对干燥过程控制要求很高。
⑴喷雾干式烟气脱硫工艺:喷雾干式烟气脱硫(简称干法FGD),最先由美国JOY公司和丹麦Niro Atomier公司共同开发的脱硫工艺,70年代中期得到发展,并在电力工业迅速推广应用。该工艺用雾化的石灰浆液在喷雾干燥塔中与烟气接触,石灰浆液与SO2反应后生成1种干燥的固体反应物,最后连同飞灰一起被除尘器收集。中国曾在四川省白马电厂进行了旋转喷雾干法烟气脱硫的中间试验,取得了一些经验,为在200~300MW机组上采用旋转喷雾干法烟气脱硫优化参数的设计提供了依据。
⑵粉煤灰干式烟气脱硫技术:日本从1985年起,研究利用粉煤灰作为脱硫剂的干式烟气脱硫技术,到1988年底完成工业实用化试验,1991年初投运了首台粉煤灰干式脱硫设备,处理烟气量644000Nm3/h。其特点:脱硫率高达60%以上,性能稳定,达到了一般湿式法脱硫性能水平;脱硫剂成本低;用水量少,无需排水处理和排烟再加热,设备总费用比湿式法脱硫低1/4;煤灰脱硫剂可以复用;没有浆料,维护容易,设备系统简单可靠。
湿法工艺
世界各国的湿法烟气脱硫工艺流程、形式和机理大同小异,主要是使用石灰石(CaCO3)、石灰(CaO)或碳酸钠(Na2CO3)等浆液作洗涤剂,在反应塔中对烟气进行洗涤,从而除去烟气中的SO2。这种工艺已有50年的历史,经过不断地改进和完善后,技术比较成熟,而且具有脱硫效率高(90%~98%),机组容量大,煤种适应性强,运行费用较低和副产品易回收等优点。据美国环保局(EPA)的统计资料,全美火电厂采用湿式脱硫装置中,湿式石灰法占39.6%,石灰石法占47.4%,两法共占87%;双碱法占4.1%,碳酸钠法占3.1%。世界各国(如德国、日本等),在大型火电厂中,90%以上采用湿式石灰/石灰石-石膏法烟气脱硫工艺流程。
石灰或石灰石法主要的化学反应机理为:
石灰法:SO2+CaO+1/2H2O→CaSO3·1/2H2O
石灰石法:SO2+CaCO3+1/2H2O→CaSO3·1/2H2O+CO2
其主要优点是能广泛地进行商品化开发,且其吸收剂的资源丰富,成本低廉,废渣既可抛弃,也可作为商品石膏回收。目前,石灰/石灰石法是世界上应用最多的1种FGD工艺,对高硫煤,脱硫率可在90%以上,对低硫煤,脱硫率可在95%以上。
传统的石灰/石灰石工艺有其潜在的缺陷,主要表现为设备的积垢、堵塞、腐蚀与磨损。为了解决这些问题,各设备制造厂商采用了各种不同的方法,开发出第二代、第三代石灰/石灰石脱硫工艺系统。
湿法FGD工艺较为成熟的还有:氢氧化镁法;氢氧化钠法;美国Davy Mckee公司Wellman-Lord FGD工艺;氨法等。
在湿法工艺中,烟气的再热问题直接影响整个FGD工艺的投资。因为经过湿法工艺脱硫后的烟气一般温度较低(45℃),大都在露点以下,若不经过再加热而直接排入烟囱,则容易形成酸雾,腐蚀烟囱,也不利于烟气的扩散。所以湿法FGD装置一般都配有烟气再热系统。目前,应用较多的是技术上成熟的再生(回转)式烟气热交换器(GGH)。GGH价格较贵,占整个FGD工艺投资的比例较高。近年来,日本三菱公司开发出1种可省去无泄漏型的GGH,较好地解决了烟气泄漏问题,但价格仍然较高。前德国SHU公司开发出1种可省去GGH和烟囱的新工艺,它将整个FGD装置安装在电厂的冷却塔内,利用电厂循环水余热来加热烟气,运行情况良好,是1种十分有前途的方法。
等离子体烟气脱硫
等离子体烟气脱硫技术研究始于70年代,目前世界上已较大规模开展研究的方法有两类:
电子束法
电子束辐照含有水蒸气的烟气时,会使烟气中的分子如O2、H2O等处于激发态、离子或裂解,产生强氧化性的自由基O、OH、HO2和O3等。这些自由基对烟气中的SO2和NO进行氧化,分别变成SO3和NO2或相应的酸。在有氨存在的情况下,生成较稳定的硫铵和硫硝铵固体,它们被除尘器捕集下来而达到脱硫脱硝的目的。
脉冲法
脉冲电晕放电脱硫脱硝的基本原理和电子束辐照脱硫脱硝的基本原理基本一致,世界上许多国家进行了大量的实验研究,并且进行了较大规模的中间试验,但仍然有许多问题有待研究解决。
海水脱硫
海水通常呈碱性,自然碱度大约为1.2~2.5mmol/L,这使得海水具有天然的酸碱缓冲能力及吸收SO2的能力。国外一些脱硫公司利用海水的这种特性,开发并成功地应用海水洗涤烟气中的SO2,达到烟气净化的目的。
海水脱硫工艺主要由烟气系统、供排海水系统、海水恢复系统等组成。
美嘉华技术
脱硫系统中常见的主要设备为吸收塔、烟道、烟囱、脱硫泵、增压风机等主要设备,美嘉华技术在脱硫泵、吸收塔、烟道、烟囱等部位的防腐蚀、防磨效果显着,现分别叙述。
应用1
湿法烟气脱硫环保技术(FGD)因其脱硫率高、煤质适用面宽、工艺技术成熟、稳定运转周期长、负荷变动影响小、烟气处理能力大等特点,被广泛地应用于各大、中型火电厂,成为国内外火电厂烟气脱硫的主导工艺技术。但该工艺同时具有介质腐蚀性强、处理烟气温度高、SO2吸收液固体含量大、磨损性强、设备防腐蚀区域大、施工技术质量要求高、防腐蚀失效维修难等特点。因此,该装置的腐蚀控制一直是影响装置长周期安全运行的重点问题之一。
湿法烟气脱硫吸收塔、烟囱内筒防腐蚀材料的选择必须考虑以下几个方面:
(1)满足复杂化学条件环境下的防腐蚀要求:烟囱内化学环境复杂,烟气含酸量很高,在内衬表面形成的凝结物,对于大多数的建筑材料都具有很强的侵蚀性,所以对内衬材料要求具有抗强酸腐蚀能力;
(2)耐温要求:烟气温差变化大,湿法脱硫后的烟气温度在40℃~80℃之间,在脱硫系统检修或不运行而机组运行工况下,烟囱内烟气温度在130℃~150℃之间,那么要求内衬具有抗温差变化能力,在温度变化频繁的环境中不开裂并且耐久;
(3)耐磨性能好:烟气中含有大量的粉尘,同时在腐蚀性的介质作用下,磨损的实际情况可能会较为明显,所以要求防腐材料具有良好的耐磨性;
(4)具有一定的抗弯性能:由于考虑到一些烟囱的高空特性,包括是地球本身的运动、地震和风力作用等情况,烟囱尤其是高空部位可能会发生摇动等角度偏向或偏离,同时烟囱在安装和运输过程中可能会发生一些不可控的力学作用等,所以要求防腐材料具有一定的抗弯性能;
(5)具有良好的粘结力:防腐材料必须具有较强的粘结强度,不仅指材料自身的粘结强度较高,而且材料与基材之间的粘结强度要高,同时要求材料不易产生龟裂、分层或剥离,附着力和冲击强度较好,从而保证较好的耐蚀性。通常我们要求底涂材料与钢结构基础的粘接力能够至少达到10MPa以上
应用2
脱硫浆液循环泵是脱硫系统中继换热器、增压风机后的大型设备,通常采用离心式,它直接从塔底部抽取浆液进行循环,是脱硫工艺中流量最大、使用条件最为苛刻的泵,腐蚀和磨蚀常常导致其失效。其特性主要有:
(1)强磨蚀性
脱硫塔底部的浆液含有大量的固体颗粒,主要是飞灰、脱硫介质颗粒,粒度一般为0~400µm、90%以上为20~60µm、浓度为5%~28%(质量比)、这些固体颗粒(特别是Al2O3、SiO2颗粒)具有很强的磨蚀性
(2)强腐蚀性
在典型的石灰石(石灰)-石膏法脱硫工艺中,一般塔底浆液的pH值为5~6,加入脱硫剂后pH值可达6~8.5(循环泵浆液的pH值与脱硫塔的运行条件和脱硫剂的加入点有关);Cl-可富集超过80000mg/L,在低pH值的条件下,将产生强烈的腐蚀性。
(3)气蚀性
在脱硫系统中,循环泵输送的浆液中往往含有一定量的气体。实际上,离心循环泵输送的浆液为气固液多相流,固相对泵性能的影响是连续的、均匀的,而气相对泵的影响远比固相复杂且更难预测。当泵输送的液体中含有气体时泵的流量、扬程、效率均有所下降,含气量越大,效率下降越快。随着含气量的增加,泵出现额外的噪声振动,可导致泵轴、轴承及密封的损坏。泵吸入口处和叶片背面等处聚集气体会导致流阻阻力增大甚至断流,继而使工况恶化,必须气蚀量增加,气体密度小,比容大,可压缩性大,流变性强,离心力小,转换能量性能差是引起泵工况恶化的主要原因。试验表明,当液体中的气量(体积比)达到3%左右时,泵的性能将出现徒降,当入口气体达20%~30%时,泵完全断流。离心泵允许含气量(体积比)极限小于5%。
高分子复合材料现场应用的主要优点是:常温操作,避免由于焊补等传统工艺引起的热应力变形,也避免了对零部件的二次损伤等;另外施工过程简单,修复工艺可现场操作或设备局部拆装修复;美嘉华材料的可塑性好,本身具有极好的耐磨性及抗冲刷能力,是解决该类问题最理想的应用技术。
脱硫技术_脱硫 -方程
SO2被液滴吸收方程
SO2(气)+H2O→H2SO3(液)
⑵ 吸收的SO2同溶液的吸收剂反应生成亚硫酸钙;
Ca(OH)2(液)+H2SO3(液)→CaSO3(液)+2H2O
Ca(OH)2 (固) +H2SO3(液)→CaSO3(液)+2H2O
⑶ 液滴中CaSO3达到饱和后,即开始结晶析出;
CaSO3(液)→CaSO3(固)
⑷ 部分溶液中的CaSO3与溶于液滴中的氧反应,
氧化成硫酸钙;
CaSO3(液)+1/2O2(液)→CaSO4(液)
⑸ CaSO4(液)溶解度低,从而结晶析出
CaSO4(液)→CaSO4(固)
SO2与剩余的Ca(OH)2 及循环灰的反应
Ca(OH)2 (固) →Ca(OH)2 (液)
SO2(气)+H2O→H2SO3(液)
Ca(OH)2 (液)+H2SO3(液)→CaSO3(液)+2H2O
CaSO3(液)→CaSO3(固)
CaSO3(液)+1/2O2(液)→CaSO4(液)
CaSO4(液)CaSO4(固)
双碱法方程
2NaOH+SO2→Na2SO3+H2O
Na2SO3+SO2+H2O→2NaHSO3
Ca(OH)2 + Na2SO3 → 2 NaOH + CaSO3
4NaHSO3+2Ca(OH)2→2Na2SO3+2CaSO3·H2O+H2O
2Na2SO3+O2 +2Ca(OH)2+4H2O→4NaOH+2CaSO4·2H2O
三 : 脱硫工艺流程
脱硫系统工艺流程
我公司脱硫系统采用国内较为先进的以焦炉煤气中自身含有氨为碱源的AS湿法脱硫工艺。该工艺流程为:从初冷器冷却后的煤气进入AS脱硫塔,由塔顶循环液喷洒吸收H2S、HCN等,脱硫后的煤气输送到下步工序。脱硫液由泵送到蒸氨塔蒸氨,冷凝氨水进入饱和器生产硫酸铵,H2S、HCN、CO等不凝性气体由罗茨风机加压送到WSA硫酸装置,经燃烧、氧化转化、冷凝等最后生成硫酸产品。
但考虑到生产LNG、甲醇,对煤气中H2S含量低于20mg/m3的严格要求,另外上了四套HPF脱硫系统。具体工艺流程如下:从冷鼓工段来的粗煤气首先进入预冷塔,使出塔煤气温度降到25-30℃之间,然后煤气进入脱硫塔下部与塔顶喷淋下来的脱硫液逆流接触洗涤后,煤气中的H2S、HCN等被脱硫液吸收后,煤气由塔顶排出,后经捕雾段除去雾滴后全部送至硫铵工段。自脱硫塔塔底流出的脱硫液经液封槽进入反应槽,再由脱硫泵加压送入再生塔底部,同时在再生塔底部鼓入压缩空气,使溶液在塔内得到再生,再生后的溶液经塔顶液位调节阀自流回到脱硫塔顶循环喷洒回用。再生过程中产生的硫泡沫由再生塔顶排至脱硫泡沫槽,在搅拌机的作用下使硫泡沫破裂,然后经泡沫泵由泡沫槽底部打入熔硫釜,经生化处理得到硫磺。
AS脱硫+HPF法湿式氧化脱硫工艺脱硫效果高,工艺操作弹性极大,脱硫稳定,可以适应原料气流量和硫化物浓度的大范围波动;同时该工艺具有布局简单,操作经济、热效高、产品价值高、能耗低等特点,是处理焦炉煤气等含硫化氢气体的最佳工艺。
四 : MDEA天然气脱硫工艺流程67
《仪陇天然气脱硫》项目书
目录
1总论 ........................................................................................................ 3
1.1项目名称、建设单位、企业性质 ................................................................................. 3
1.2编制依据 ......................................................................................................................... 3
1.3项目背景和项目建设的必要性 ..................................................................................... 3
1、4设计范围 ...................................................................................................................... 5
1、5编制原则 ...................................................................................................................... 5
1.6遵循的主要标准、规范 ................................................................................................. 8
1.7 工艺路线 ........................................................................................................................ 8
2 基础数据 ............................................................................................... 8
2.1原料气和产品 ................................................................................................................. 8
2.2 建设规模 ........................................................................................................................ 9
2.3 工艺流程简介 ................................................................................................................ 9
2.3.1醇胺法脱硫原则工艺流程: ............................................................................... 9
2.3.2直流法硫磺回收工艺流程: ..............................................................................10
3 脱硫装置 ..............................................................................................11
3.1 脱硫工艺方法选择 ...................................................................................................... 11
3.1.1 脱硫的方法 ...................................................................................................... 11
3.1.2醇胺法脱硫的基本原理 .....................................................................................12
3.2 常用醇胺溶液性能比较 .............................................................................................. 13
3.1.2.1几种方法性质比较 ..........................................................................................14
3.2醇胺法脱硫的基本原理 ............................................................................................... 17
3.3主要工艺设备 ............................................................................................................... 18
3.3.1主要设备作用 ...................................................................................................18
3.3.2运行参数 ..........................................................................................................19
3.3.3操作要点 ..........................................................................................................20
3.4乙醇胺降解产物的生成及其回收 ............................................................................... 21
3.5脱硫的开、停车及正常操作 ....................................................................................... 22
3.5.1乙醇胺溶液脱硫的开车 .....................................................................................22
3.5.2保证乙醇胺溶液脱硫的正常操作 .......................................................................22
3.6胺法的一般操作问题 ................................................................................................... 23
3.6.1胺法存在的一般操作问题 ..................................................................................23
3.6.2操作要点 ..........................................................................................................24
3.7选择性脱硫工艺的发展 ............................................................................................... 25
4 节能 ..................................................................................................... 25
4.1装置能耗 ....................................................................................................................... 25
装置中主要的能量消耗是在闪蒸罐、换热器和再生塔。 ............................................. 25
4.2节能措施 ....................................................................................................................... 25
5 环境保护 ........................................................................................... 26
5.1建设地区的环境现状 ................................................................................................... 26
5.2、主要污染源和污染物 ................................................................................................ 26
5.3、污染控制 .................................................................................................................... 26
6 物料衡算与热量衡算........................................................................... 28
6.1天然气的处理量 ........................................................................................................... 28
7.天然气脱硫工艺主要设备的计算 ......................................................... 33
7.1MDEA吸收塔的工艺设计............................................................................................ 33
7.1.1选型 .................................................................................................................33
7.1.2塔板数 ..............................................................................................................33
7.1.3塔径 .................................................................................................................34
7.1.4堰及降液管 .......................................................................................................36
7.1.5浮阀计算 ..........................................................................................................37
7.1.6 塔板压降..........................................................................................................37
7.1.7塔附件设计 .......................................................................................................39
7.1.8塔体总高度的设计 ............................................................................................40
7.2解吸塔 ........................................................................................................................... 41
7.2.1 计算依据..........................................................................................................41
7.2.2塔板数的确定 ...................................................................................................41
7.2.3解吸塔的工艺条件及有关物性的计算 ................................................................42
7.2.4解吸塔的塔体工艺尺寸计算 ..............................................................................43
8参数校核 .............................................................................................. 44
8.1浮阀塔的流体力学校核 ............................................................................................... 44
8.1.1溢流液泛的校核 ................................................................................................44
8.1.2液泛校核 ..........................................................................................................44
8.1.3液沫夹带校核 ...................................................................................................45
8.2塔板负荷性能计算 ....................................................................................................... 45
8.2.1漏液线(气相负荷下限线) ..............................................................................45
8.2.2 过量雾沫夹带线 ...............................................................................................45
8.2.3 液相负荷下限...................................................................................................46
8.2.4 液相负荷上限...................................................................................................46
8.2.5 液泛线 .............................................................................................................46
9 附属设备及主要附件的选型和计算 .................................................... 47
10.心得体会 ............................................................................................ 49
11.参考文献............................................................................................. 50
1总论
1.1项目名称、建设单位、企业性质
项目名称:天然气脱硫
建设单位:中石油仪陇净化厂
企业性质:国营企业
1.2编制依据
天然气可分为酸性天然气和洁气。酸性天然气指含有显著量的硫化物和CO2等酸性气体,必须经处理后才能达到管输标准或商品气气质指标的天然气。洁气是指硫化物和CO2含量甚微或根本不含,不需要净化就可以外输和利用的天然气。天然气中存在的硫化物主要是H2S,此外还可能含有一些有机硫化物,如硫醇、硫醚、COS及二硫化碳等;除硫化物外,二氧化碳也是需要限制的指标。酸性天然气的危害有:酸性天然气在水存在的条件下会腐蚀金属;污染环境;含硫组分有难闻的臭味、剧毒;硫可能使下游工厂的催化剂中毒;H2S可对人造成伤害;CO2含量过高会使天然气热值达不到要求。
1.3项目背景和项目建设的必要性
天然气是一次能源中最为清洁、高效、方便的能源,不仅在工业与城市民用燃气中广泛应用,而且在发电业中也越来越重要作用,近20年来在我国呈现出快速发展的态势。从西气东输和川气东送为标志的天然气管道工程建设到2009年11月份气荒,都促进了天然气市场的发展。
煤炭在我国一次能源消费中的比例将近70%,以煤为主的能源消费结构二氧化碳排放过多,对环境压力较大。合理利用天然气,充分净化天然气,可以优化能源消费结构,改善大气环境,提高人民生活质量,对实现节能减排目标、建设环境友好型社会具有重要意义。
天然气是指自然界中天然存在的一切气体,包括大气圈、水圈、生物圈和
岩石圈中各种自然过程形成的气体。而人们长期以来通用的“天然气”是从能量角度出发的狭义定义,是指气态的石油,转指在岩石圈中生成并蕴藏于其中的以低分子饱和烃为主的烃类气体和少量非烃类气体组成的可燃性气体混合物。它主要存在于油田气、气田气、煤层气、泥火山气和生物生成气中。天然气是一种多组分的混合气体,主要成分是烷烃,其中甲烷占绝大多数,另有少量的乙烷、丙烷和丁烷,此外一般还含有硫化氢、二氧化碳、氮和水气,以及微量的惰性气体,如氦和氩等。在标准状况下,甲烷至丁烷以气体状态存在,戊烷以上为液体。
从矿藏中开采出来的天然气是组分非常复杂的烃类混合物,且含有少量的非烃类杂质。其中,非烃类杂质常常含有H2S、CO2和有机硫化物。由于水的存在,这些气体组分将生成酸或酸溶液,造成输气管道和设备的严重腐蚀。天然气中的硫化物及其燃烧物会破坏周围环境,损害人类健康。而像H2S和硫醇这样的硫化物, 并使之转化为可供工业应用的元素硫,便构成一条天然气工业中普遍采用的净化、回收硫的基本技术路线。此外,当硫磺回收装置的尾气不符合大气排放标准时,还应建立尾气处理装置。因此,天然气中的H2S量受到严格限制,开采出的天然气往往须经脱硫预处理,以满足传输及使用要求。欧美发达国家制定的商品天然气气质标准规定:H2S控制含量在5mg/m3天然气左右;总硫控制含量为100mg/m3天然气(以硫计)左右;我国国家标准规定:Ⅰ类商品天然气H2S含量≤6 mg/m3,总硫含量≤100 mg/m3天然气(以硫计)。故而一个完整的天然气脱硫厂应包括脱硫装置、硫磺回收装置和尾气处理装置。 天然气可分为酸性天然气和洁气。酸性天然气指含有显著的硫化物和CO2等酸性气体必须经处理后才能达到管输标准或商品气气质指标的天然气。洁气是指硫化物和CO2含量甚微或根本不含,不需净化就可外输或使用的天然气。来自地下储层的天然气通常不同程度地含有H2S、CO2和有机硫化物(RSH、COS、RSSR,)等酸性组分,在开采、集输和处理时会造成设备和管道腐蚀;而且含硫组分往往有毒、有害并具有难闻的臭味,会污染环境和威胁人身安全(少量硫化氢就具有剧毒,虽然硫化氢在浓度极低时就能检测到,但由于嗅疲劳,在接触后几分钟内就会丧失嗅觉,从而无法感觉到硫化氢的危险浓度。吸入浓度为几百ppm的硫化氢可能导致急性中毒,而且,虽然这种气体具有刺激性,但血液中吸收硫化氢所产生的全身效应会掩盖其刺激作用);
当天然气用作化工原料时,还会引起催化剂中毒;同时,CO2的含量过高将降低天然气的热值。
综上所述,天然气在使用前必须进行脱硫处理,严格控制酸性气体的含量,使其硫含量满足GB17320-1999天然气标准规定的天然气的技术指标,才能成为合格的使用天然气。
1、4设计范围 (1)天然气脱硫的必然性
(2)天然气脱硫的方法及工艺路线的选择
(3)物料流程图
(4)工艺流程图
(5)脱硫装置
(6)建设规模
1、5编制原则 通过加工的天然气所达到的气质指标,各国各地区都不同,这是由于天然气资源和矿藏处理水平、供销状况及有关的经济政策等各不相同所造成的。
由于化工生产所需要的原料气对有害物质特别是硫及其化合物的含量要求比较严格(硫含量一般为1-2mg/m3),天然气通常需要经过二次处理才能符合要求,而且这部分气量相对较小,故在制定商品天然气气质指标是多以符合燃料要求为依据,主要从保证天然气在输配系统中的安全运行,减少设备、管线的腐蚀,满足环境保护和卫生以及良好的燃料性能等方面规定对商品天然气的质量要求。随着天然气在能源结构中的比例上升,输气管道压力升高,距离增长,对气质的要求也趋于严格。在西方发达国家,气质指标除了管输指标外,往往还必须根据用户与公司签订的销售合同的有关条款来实行质量要求,以满足用户的需要。
商品天然气气质指标主要有:
(1)最小热。值为了使天然气用户能适当确定其加热设备,必须确定最小热值。这项规定主要要求控制天然气中的N2和CO2等不可燃气体的含量。
MDEA天然气脱硫工艺流程67_脱硫工艺
(2)含硫量。主要是为了控制天然气的腐蚀性和出于对人类自身健康和安全的考虑,常以H2S含量或总硫(H2S及其他形态)含量来表示。
(3)烃露点。烃露点即在一定压力条件下天然气中析出的第一滴液烃时的温度,它与天然气的压力和组成有关。为了防止天然气在输配管线中有液烃凝结,目前许多国家都对商品天然气规定了脱油除尘的要求,规定在一定条件下天然气的最高允许烃露点。
(4)水露点与含水量。在地层温度和压力条件下,水在天然气中通常以饱和水蒸汽的形式存在,水蒸气的存在往往给天然气的输集带来了一系列的危害。因此,规定天然气的含水量是十分必要的。天然气的含水量以单位体积天然气中所含的水汽量来表示的,有时也用天然气的水露点来表示。天然气的水露点是指在一定的压力条件下,天然气与液态水平衡时(此时,天然气的含水量为最大含水量,即饱和含水量)的温度。一般要求天然气水露点比输气管线可能达到的最低温度还低5-6℃。
此外,往往还要求输送温度不超过49℃,对输送压力无严格要求。
GB 17820-1999依据不同用户的要求并结合我国天然气资源的实际组成,将商品天然气分成三类。一类和二类天然气主要用作民用燃料,为了防止输配系统的腐蚀和保证居民健康,分贝规定其硫含量不大于6mg/m(CHN)和20mg/m(CHN):三类天然气主要作为工业原料和燃料。GB17820-1999同时规定高位发热量大于31.46MJ/m3(CHN),二氧化碳体积分数不大于3%,在天然气交接点的压力和温度条件下,天然气的水露点应比最低环境温度低5℃。考虑个别用户对天然气质量有不同要求,GB 17820-1999的附录同时规定;在满足国家有关安全卫生等标准的前提下,对上述三个类别以外的天然气,允许供需双方合同或协议来确定其具体质量要求。
我国商品天然气气质技术标准如下表:
表 1 商品天然气气质技术标准 (GB17820-1999)
3
3
此外,按照用途不同,典型天然气气质指标见表2。
表2 典型天然气气质指标
注:1.H2S+羟基硫+有机硫化合物
2.取决于用途
3.体积与净化气体优化热量之比
1.6遵循的主要标准、规范
GB 16297-1996 《大气污染物综合排放标准》 GB 17820-1999 《商品天然气的技术标准》 SY/T6538-2002 《配方型选择性脱硫溶剂标准》
SY/T6537-2002 《天然气净化厂气体及溶液分析方法标准》
1.7 工艺路线
开采出来的天然气中含有硫化氢和二氧化碳等酸性气体,在使用过程中会造成许多危害,所以在使用前必须进行脱硫脱碳处理。
一般的化学吸收法通过吸收剂溶液吸收天然气中的酸性组分,大部分酸性组分被吸收剂溶液所吸收,残余的酸性组分需进一步吸收分离,以达到商品气气质指标的要求。含有酸性组分的溶液需要输入再生装置中进行再生回收,以求得吸收剂的循环使用。一般的化学吸收法有吸收、闪蒸、换热和再生四部分组成。
2 基础数据
2.1原料气和产品
1) 原料气组成
注:1)原料气不含有机硫
2)原料气处理量 307?103m3/d 3) 原料气温度 30~36 ℃ 4)原料气压力 2.05-2.25MPa(g)
2.2 建设规模
仪陇龙岗净化厂建设规模为307?103m3/d。
2.3 工艺流程简介
2.3.1醇胺法脱硫原则工艺流程:
醇胺法工艺的基本流程主要有吸收、闪蒸、换热和再生四部分组成。
含酸性组分的天然气经入口分离器除去液固杂质后进入吸收塔底部,由下而上与醇胺溶液逆流接触,脱出其中的酸性组分。达到要求的净化器离开吸收塔顶部,井出口分离器除去携带的醇胺液滴后出装置。
吸收了酸气的醇胺溶液(通常称为富液)由吸收塔底部流出后降至一定压力进入
闪蒸罐,是富液中溶解和夹带的烃类闪蒸出来,闪蒸汽可用作装置的燃料气。闪蒸后的富液经过滤器进入贫/富液换热器,与已完成再生的热醇胺(简称贫液)换热而被加热,然后进入在低压下操作的再生塔顶部。
在再生塔中富液首先在塔顶闪蒸处部分酸性组分,然后自上而下流动与在重沸器中加热气化的气体(主要为水蒸气)接粗,将溶液中其余的酸性组分进一步汽提出来。因此,出再生塔的溶液为贫液,只含有少量未汽提出的残余酸性气体。离开重沸器的热贫液经贫/富液换热器回收热量后,再经过溶液冷却器的进一步冷却至冷却至适当温度,然后由溶液循环泵送至吸收塔顶部,完成溶液循环。
离开再生塔顶部的酸性组分和水蒸气进入冷却器,以冷凝分出大部分水蒸气,冷凝液作为回流返回再生塔顶部,以回收被酸性气流带出的醇胺蒸汽,酸气送至硫磺回收装置或其他气体处理设施进一步处理。
2.3.2直流法硫磺回收工艺流程:
在直流法中,全部酸气进入反应炉,要求严格配给空气量,以使酸气中的全部烃完全燃烧,而H2S仅有l/3氧化成SO2,使剽余2/3的H2S与氧化成的SO2在理想的配比下进行催化转化,以获取更高的转化率。反应炉温度高达1100一1600℃,此时酸气中H2S约有60%一70%转化成硫,含硫蒸气的高温气体经余热钢炉回收热量后进入一级冷凝器,再次回收热量并分离出液态硫,出一级冷凝器的气相进入一级再热器,使其在进一级转化器前达到所需要的反应温度,然后进人一级转化器,在已活化的催
MDEA天然气脱硫工艺流程67_脱硫工艺
化剂上反应,由于反应放热,出口气温度明显升高,经二级冷凝器回收热量并分离出液态硫之后的气相,经二级再热器再热达到需要的温度,进入二级转化器,催化转化后温度升高,经三级冷凝器回收热量并分离出液态硫,分出液态疏后的气相进入第三级再热器,再热后进入三级转化器,使H2S和SO2最大限度地转化为硫,从三级转化器出来的气相经四级冷凝器冷却以除去最后生成的硫。分离出液态疏后的尾气通过捕集器,进一步捕集液态硫后进入尾气处理装置进一步处理后排放。各级冷凝器及捕集器中分离出来的液态硫流人硫储罐,经成型后即为硫磺产品。
3 脱硫装置
3.1 脱硫工艺方法选择
3.1.1 脱硫的方法
目前,国内外已见的天然气脱硫方法名目繁多,不下数十种。如果以脱硫剂的状态来分,则天然气脱硫法可分为干法和湿法两大类。
干法---采用固体型的脱硫吸附剂,这类固体物质包括天然泡沸石、分子筛和海绵状氧化铁等。
湿法---采用各类液体溶液脱硫剂。此法多用于高压天然气中酸性气体组分含量较多的情况湿法本身又可按条件分为:化学吸收法、物理吸收法、复合法和直接氧化法。
化学吸收法基于可逆化学反应。吸收剂在吸收塔内与H2S和CO2进行反应,在解吸塔内用提高温度或降低压力的办法使向相反方向进行。各种胺溶液是应用品广泛的脱硫吸收剂。除了各种醇胺法以外,碱性盐溶液和氨基酸盐法亦属于化学吸收脱硫法。
物理吸收法是基于吸收剂的选择性吸收来分离抽取天然气中酸性组分,其操作类似于天然气工厂中油吸收法。在物理吸收过程中,可采用N-甲基吡咯烷酮、碳酸丙烯酯、丙酮、甲醇等作为吸收剂。由于吸收剂的吸收能力实际上与气相中酸性组分的分压成正比,故而本法对处理高含酸性组分的天然气特备有效。
复合法同时使用混合的化学和物理吸收剂。本法中最得以广泛应用的是Sulfinol法,其中使用环丁砜和任一化学吸收剂相组合的溶液作为脱硫剂。Sulfinol
溶液通常是有环丁砜、二异丙醇胺和水组成。在确定Sulfinol砜胺溶液配比时,应考虑依据使用条件不同而异。
醇胺法是目前最常用的天然气脱硫脱碳方法。据统计,20世纪90年代美国采用化学溶剂法的脱硫脱碳装置处理量约占总处理量的72%,其中有绝大多数是采用醇胺法。
20世纪30年代最先采用的醇胺法是三乙醇胺(TEA),因其反应能力和稳定性差已不再采用。目前,主要采用的是一乙醇胺(MEA)、常规的二乙醇胺(DEA)、二异丙醇胺(ADIP)、二甘醇胺(DGA)和甲基二乙醇胺(MDEA)等溶剂。
醇胺法适用于天然气中酸性组分含量低的场合。由于醇胺法使用的是醇胺水溶液,溶液中含水可使被吸收的重烃降低至最少程度,故非常适用于重烃含量高的天然气脱硫脱碳。MDEA等醇胺溶液还具有在CO2存在下选择性脱出H2S的能力
醇胺法的缺点是有些醇胺与COS和CS2的反应时不可逆的,会造成那个溶剂的化学降解损失,故不宜用于COS和CS2含量高的天然气脱硫脱碳。醇胺还具有腐蚀性,与天然气中的H2S和CO2等会因其设备腐蚀。此外,醇胺作为脱硫脱碳溶剂,其富液(即吸收了天然气中酸性组分后的溶液)在再生时需要加热,不仅能耗较高,而且在高温下再生时也会发生热降解,所以损耗较大。
由于醇胺法的吸收能力较强,且本设计中,在脱除H2S的同时需脱除相当量的CO2,即要求选择性脱硫,而原料气中有不含有机硫,故选择醇胺法来进行脱硫脱碳处理。
3.1.2醇胺法脱硫的基本原理
乙醇胺是无色的液体,常压下沸点为170℃,比重为1.019 g/cm。它是一种有机碱溶液,它的碱性与氨相似,是氨的衍生物。
乙醇胺结构始终至少有一个氨基,这个氨基提供了在水中的碱度,促使对于酸性气体H2S、CO2有很高的吸收能力。乙醇胺的结构式中还有一个烃基,这个烃基的作用可以降低化合物的蒸汽压,减少气相中乙醇胺的损失,并且增加了在水中的溶解度,使乙醇氨可按任意比与水互溶。乙醇胺吸收H2S、CO2时,生成硫化物、酸式硫化物、碳酸盐、酸式碳酸盐,其反应式如下:
???(RNH)S2RNH2?H2S???32
3
?RNH3?2S
???2RNHHS?H2S???3
???(RNH)CO 2RNH2?H2O?CO2???323
???2RNHHCO (RNH3)2CO3?H2O?CO2???33???RNHCOONHR2RNH2?CO2???2
反应方程式中R?CH3CH2OH?
乙醇胺吸收反应是放热反应,从化学平衡观点来看,温度愈低,愈有利于吸收反应。所以温度一般控制在25-40℃为宜。
吸收了H2S、CO2的乙醇胺溶液,当温度升高至105℃以上,则生成物就要分解,生成反应物,这就是乙醇胺的再生。再生温度的提高对溶液再生是有好处的,因为温度提高后,溶液表面上酸性气体的分压迅速增加。
提高压力有利于吸收,同时也提高了H2S的分压,增大了吸收的推动,提高了溶液的吸收能力。
富液再生的压力一般为常压,因为乙醇胺溶液再生是在该压力下塔底溶液沸腾温度下再生的,压力提高后,相对应的溶液沸腾温度亦高,但由于压力高而相对应的H2S、CO2的分压亦高了。此时,H2S、CO2的分压增加而使硫化物、碳酸盐离解降低的作用比升高温度而使离解增加的作用更为显著,因此再生的压力一般为常压。
3.2 常用醇胺溶液性能比较
醇胺法特别适用于酸气分压低和要求净化气中酸气含量低的场合。由于采用的是水溶液可减少重烃的吸收量,故此法更适合重烃的气体脱硫脱碳。
通常,MEA法、DEA法、DGA法有成为常规醇胺法,基本上可同时脱除气体中的H2S、CO2;MDEA法和DIPA法又称为选择性醇胺法,其中MDEA法是典型的选择性脱H2S法,DIPA法在常压也可选择性的脱除H2S。此外,配方溶液目前种类繁多,性能各不相同,分别用于选择性脱H2S,在深度或不深度脱除H2S的情况下脱除一部分或大部分CO2,深度脱除CO2,以及脱除COS等。
醇胺分子结构至少有一个羟基和一个胺基。羟基:可降低化合物的蒸汽压,增加醇胺在水中的溶解度,可配制成水溶液。胺基:水溶液提供碱度,促进对酸性组分的吸收。醇胺与H2S、CO2的主要反应如下:
伯胺:
???RNH??HS? RNH2?H2S???3
(瞬间反应)
???RNH??RNHCOO? 2RNH2?CO2???3(中速反应)
???RNH??HCO? (慢反应) RNH2?CO2?H2O???33
仲胺:
???RNH??HS?R2NH?H2S???22
(瞬间反应)
?? ??? 2RNH2?CO2??(中速反应) RNH?RNCOO?222
???RNH??HCO?R2NH?CO2?H2O???223
(慢反应)
叔胺:
'
???RR'NHR2RN?H2S???2
?
?HS
?
(瞬间反应)
R2R'N?CO2 (不反应)
???RR'NH??HCO? (慢反应) R2R'N?CO2?H2O???23
醇胺与H2S、CO2的主要反映均为可逆反应。当酸性组分P高或T低时,反应向右进行,贫液从原料气中吸收酸性组分(正反应),并且放热。当酸性组分P低或T高时,反映向左进行,富液将酸性组分释放出来使溶液再生(逆反应),并且吸热。
3.1.2.1几种方法性质比较
主要天然气脱硫溶剂的性质
性质
分子式 相对分子质量
20
相对密度d20
MEA
HOC2H4NH2 61.08 1.0179 10.2 170.4 93.3 1.4539 28
DEA DIPA MDEA (HOC2H4)2NH (HOC3H6)2NH (HOC2H4)2NCH3 105.14 1.0919 28 268.4 137.8 1.4776 <1.33
133.19 0.989 42 248.7 123.9 1.4542(45) <1.33
119.17 1.418 -14.6 230.6 126.7 1.469 <1.33
环丁砜 C4H8SO2 120.14 1.2614 28.8 285 176.7 1.4820(30)
0.6
凝点/℃ 沸点/℃
闪点(开杯)/℃ 折射率
蒸汽压(20/℃)/Pa 黏度mPa.s
24.1(20/℃) 380(20/℃) 198(45/℃) 101(45/℃) 10.286(30/℃)
比热容 [kJ/(kg.℃)] 2.54(20/℃) 2.51(20/℃) 2.89(30/℃) 2.24(15.6/℃) 1.34(25/℃) 热导率 [W/(m.K)] 0.256 0.22 - 0.275(20/℃) -
1.92
汽化热 (kJ/kg) 1.56 (9.73KPa) 1 (9.73KPa) 1.21 (101.3KPa) -
(101.3KPa)
水中溶解度
完全互溶 0.964 0.87 完全互溶 完全互溶
(20/℃)
①一乙醇胺(MEA)
MEA可用于低吸收压力和净化气质质量指标要求严格的场合。MEA可从气体中同时脱除H2S和CO2因此没有选择性。净化气中H2S的浓度可低达5.7mg/m3。在中低压情况下CO2浓度可低达100×10-6(体积分数)。MEA也可脱除COS、CS2,但是需要采用复活釜,否则反应是不可逆的。即就是有复活釜,反应也不能完全可逆,故会导致溶液损失和在溶液中出现降解产物的积累。MEA的酸气负荷上限通常为0.3-0.5mol酸气/mol MEA,溶液质量浓度一般应限定在10%-20%。如果采用缓蚀剂,则可使溶液浓度和酸气负荷显著提高。由于MEA蒸汽压在醇胺类中最高,故在吸收塔、再生塔中蒸发损失量最大,但可采用水洗的方法降低损失。
②二乙醇胺(DEA)
DEA不能像MEA那样在低压下使气体处理后达到输管要求,而且也没有选择性。如果酸气分压高而且总压高,则可采用具有专利权的SNPA-DEA法。此法可用于高压且具有较高H2S/CO2比的酸气含量高的气体。专利上所表示的酸气负荷为0.9-1.3mol酸气/molDEA。
与MEA相比,DEA的特点为:DEA的碱性和腐蚀性较MEA弱,故其溶液浓度和酸气负荷较高,溶液循环量、投资和操作费用都较低;由于DEA生成不可再生的降解产物数量较少,故不需要复活釜;DEA与H2S和CO2的反应热较小,故溶液再生所需的热量较少;DEA与COS、CS2反应生成可再生的化合物,故可在溶液损失很小的情况下部分脱除COS、CS2;蒸发损失较少。
③三甘醇胺
DGA是伯醇胺,不仅可脱除气体和液体中的H2S和CO2,而且可以脱除COS和RSH,故广泛用于天然气和炼厂气脱硫脱碳。DGA可在压力低于0.86MPa下将气体中的H2S脱除至5.7 mg/m3。DGA溶液浓度在50%时的凝点为—34℃,故可适用于高寒地区。由于降解反应速率达,所以DGA系统需要采用复活釜。此外,它与CO2、
MDEA天然气脱硫工艺流程67_脱硫工艺
COS 的反应时不可逆的。与MEA、DEA相比,DGA对烯烃、重烃和芳香烃的吸收能力更强。因此,在DGA脱硫脱碳装置的设计中应采用合适的活性碳过滤器。
与MEA相比,DGA的特点为:溶液质量浓度可达50%-70%,而MEA溶液浓度仅为15%-20%;由于溶液浓度高,所以溶液循环量小;重沸器蒸汽耗量低。
④甲基二乙醇胺
MDEA是叔醇胺,可在中、高压下选择性脱除H2S以符合净化气的质量指标或管输要求。但是,如果净化气中的CO2含量超过允许值,则需进一步处理。
选择性脱除H2S的优点是:由于脱除的酸气量减少而使溶液循环量降低;再生系统的热负荷低;酸气中的H2S/CO2摩尔比可高达含硫原料气的10-15倍。由于酸气中H2S浓度较高,有利于硫磺回收。
此外,叔醇胺与CO2的反应时反应热较小的酸碱反应,故再生时需要的热量较少,因而用于大量脱除CO2是很理想的。这也是一些适用于大量脱除CO2的配方溶液的主剂是MDEA的原因所在。
采用MDEA溶液选择性脱硫不仅由于循环量低而可降低能耗,而且单位体积溶液再生所需蒸汽量也显著低于常规醇胺法。此外,选择性醇胺法因操作的气液比较高而吸收塔的液流强度较低,因而装置的处置量也可提高。
⑤二异丙醇胺
它是仲胺,对H2S具有一定的选择性,与CO2、COS发生质变反应的能力大于MEA、DEA和DGA。二异丙醇胺可用于从液化石油气中脱除H2S和COS。
⑥配方溶液
配方溶液是一种新的醇胺溶液系列,与大多数醇胺溶液相比,由于采用配方溶液可减少设备尺寸和降低能耗而广为应用,目前常见的配方溶液产品有DOW化学公司的CAS/SPECTM,联碳公司的UCARSOLTM,Huntsman公司的TEXTREATTM等。配方溶液通常具有比MDEA更好的优越性。有的配方溶液可以选择性脱除H2S低至4×10-6(体积分数),而只脱除一小部分CO2;有的配方溶液则可以从气体中深度脱除CO2以符合深冷分离工艺的需要;有的配方溶液还可在选择性脱除H2S低至4×10-6(体积分数)的同时,将高CO2含量气体的CO2脱除至2%。
⑦空间位阻胺
从分子水平上设计的脱硫剂指在氮原子上带有一个或多个具有空间位阻结构的非链状取代基团的醇胺类化合物。通过基团的空间位阻效应和碱性来控制胺与CO2的
反应,有选择性地脱硫、脱碳。天然气酸性组分脱除工艺与脱水工艺相似。
3.2醇胺法脱硫的基本原理
乙醇胺是无色的液体,常压下沸点为170℃,比重为1.019 g/cm3。它是一种有机碱溶液,它的碱性与氨相似,是氨的衍生物。
乙醇胺结构始终至少有一个氨基,这个氨基提供了在水中的碱度,促使对于酸性气体H2S、CO2有很高的吸收能力。乙醇胺的结构式中还有一个烃基,这个烃基的作用可以降低化合物的蒸汽压,减少气相中乙醇胺的损失,并且增加了在水中的溶解度,使乙醇氨可按任意比与水互溶。乙醇胺吸收H2S、CO2时,生成硫化物、酸式硫化物、碳酸盐、酸式碳酸盐,其反应式如下:
???(RNH)S2RNH2?H2S???32
?RNH3?2S
???2RNHHS?H2S???3
???(RNH)CO 2RNH2?H2O?CO2???323
???2RNHHCO (RNH3)2CO3?H2O?CO2???33???RNHCOONHR2RNH2?CO2???2
反应方程式中R?CH3CH2OH?
乙醇胺吸收反应是放热反应,从化学平衡观点来看,温度愈低,愈有利于吸收反应。所以温度一般控制在25-40℃为宜。
吸收了H2S、CO2的乙醇胺溶液,当温度升高至105℃以上,则生成物就要分解,生成反应物,这就是乙醇胺的再生。再生温度的提高对溶液再生是有好处的,因为温度提高后,溶液表面上酸性气体的分压迅速增加。
提高压力有利于吸收,同时也提高了H2S的分压,增大了吸收的推动,提高了溶液的吸收能力。
富液再生的压力一般为常压,因为乙醇胺溶液再生是在该压力下塔底溶液沸腾温度下再生的,压力提高后,相对应的溶液沸腾温度亦高,但由于压力高而相对应的H2S、CO2的分压亦高了。此时,H2S、CO2的分压增加而使硫化物、碳酸盐离解降低的作用比升高温度而使离解增加的作用更为显著,因此再生的压力一般为常压。
主要脱硫方法的技术特点和应用领域 项目 醇胺含量/%
硫化氢含量/(mg/m3) 二氧化碳含量/% 酸性气体负荷(mol/mol) 选择脱硫能力 能耗 腐蚀性 醇胺降解 脱有机硫能力 烃溶解
国内已应用领域
MEA ≤ 15 <5 0.005 < 0.35 无 高 强 严重 差 少 天然气、炼厂
气
DEA 20~30 <5 0.005~0.02 0.3~0.8 几乎无 较高 强 有 差 少 炼厂气
砜胺--Ⅱ 30~45 <5 0.005~0.02 0.3~0.8
无 低 较弱 有 好 多
MDEA 20~50 <5~20
有 低 较弱 微 差 少
天然气、合成天然气、炼厂气、克劳
气 斯尾气
3.3主要工艺设备
3.3.1主要设备作用
A、原料气分离器
作用:分离原料气夹带的固体或液烃。如砂子、井下作业用的化学药剂等。 类型:卧式或立式分离器,内装金属网除沫器。 B、吸收塔
作用:气液传质场所,酸性组分转入醇胺液中。 类型:填料塔或板式塔,目前多采用浮阀塔。 C、闪蒸罐
作用:尽可能地解吸出富液所溶解的烃类。 类型:多采用卧式罐以保证足够的闪蒸面积。 D、过滤器
作用:去除胺液中固体和降解产物。 类型:固体过滤器、活性炭过滤器。 E、贫/富溶液换热器
作用:冷却贫液,回收的热量,同时提高富液的T。 类型:多采用管壳式,富液走管程。 F、解吸塔(再生塔)
作用:对富醇胺液进行再生,恢复溶液的净化能力。 类型:用与吸收塔相同的塔型。
3.3.2运行参数
A、吸收塔
为防止溶液起泡、液泛及夹带,空塔气速不宜过高,最大空塔气速由Souders-Brown公式计算:
ug?0.0762(?L??g)/?g
??
0.5
操作气速应降低25%~35%;降液管内液体流速一般取0.08~0.1m/s。 富液T不宜过高,否则发生解吸,入塔气体T≤38℃。 为防止重烃凝析,贫液入塔T应比原料气T高1~5℃。 B、再生塔
再生塔蒸气耗量一般为0.12-0.18t/m3醇胺液,重沸器的最高T为120℃。 再生塔顶酸性气体中烃类含量应<1%-2%。 塔顶的回流比(水蒸汽量/酸气量)一般为3:1-1:1。 C、富液换热和胺冷却
为减轻腐蚀和减少富液中酸气解吸,富液和贫液不需最大限度地换热。离开换热器的富液温度大多在82~94℃。为减少管线和换热器腐蚀,醇胺液流动速度应<0.6~1.0m/s;富液走管程。贫胺液冷却器的冷却方式:空冷、水冷、空冷+水冷。贫液一般走壳程。 D、富液闪蒸罐
闪蒸操作p:0.5MPa;操作T:45~60℃;闪蒸停留时间:3~5min。
3.3.3操作要点
A、保持溶液清洁
防止各种杂质进入溶液,尽量除去杂质或降解产物。 a.原料气分离 b.溶液过滤 c.溶剂复活
使降解的醇胺尽可能复原,使热稳定的盐类释放出游离醇胺,除去不能复活的降解产物。
MEA采用侧线蒸馏复活,DEA采用活性炭吸附复活,砜胺液的复活要经过减压蒸馏、加碱处理、白土处理等。
d.控制溶液发泡注阻泡剂(消泡剂)加以控制,主要有两类: 高分子醇类:控制非离子型的发泡物质。 硅酮类高分子化合物:控制离子型发泡物质。 B、加强防腐措施
a.合理的设计、溶液过滤和复活; b.避免氧进入装置;
作用:防止胺液与氧接触生成不可再生的化学降解产物,导致设备腐蚀和溶液发泡。
H2NCH2CH2OH
MEA
oxalicacid
H2NCH2H2NCH2
2
glyoxylicacid
HOCH2
氧还能氧化H2S生成元素S,硫与链烷醇胺反应生成二硫代氨基盐类、硫脲类、多硫化合物类和硫代硫酸盐类。
方法:惰性气(如N2)保护,对储罐、低位罐进行气封。 c.正确的开工、停工操作;
MDEA天然气脱硫工艺流程67_脱硫工艺
如装置开工前应彻底清除系统中的氧。
d.合理的酸气负荷;
e.使用缓蚀剂;
f.再沸器中溶液T与所用蒸汽T应尽可能低;
g.除去悬浮固体与分解产物;
h.避免用高温热载体,使金属壁面的温度较低。
C、补充水分
原因:出吸收塔净化气、出再生塔酸气含以及闪蒸气会带走胺液中的水分。 方式:可以回流一起打入汽提塔内;也可打入吸收塔顶的水洗塔板上。
D、降低操作成本
a.合理的再生温度和回流比;
b.加强闪蒸;
尽可能闪蒸出富液中被吸收的烃类(约为原料气1%~5%,作为装置燃料气用。 c.回收能量。
设置富液能量回收泵(水力能量回收透平)是一项有效措施,对于在高压下运转的装置更为有利。
目前,在天然气净化工业中应用的选择性脱硫溶剂主要为:MDEA法、砜胺法、空间位阻胺法。
优点:不仅具有腐蚀较轻微、不易降解变质等,而且能选择性的吸收H2S。
3.4乙醇胺降解产物的生成及其回收
乙醇胺在脱硫过程中会产生一些降解产物,即产生不可逆反应的杂质。其主要方式如下:
1.氧气进入了胺系统,胺和氧反应会被迅速氧化并生成有腐蚀性的有机酸。同时也会生成硫代硫酸盐,生成的硫酸盐可以加强碱中和,胺被游离出来。
2.和天然气里的某些硫化物COS、CS2反应,生成在再生温度下不能发生分解的化合物,但这些化合物可以加强碱将乙醇胺回收下来。
3.胺液过热分解或在高温下生成胺的衍生物二胺类等物质,这些产物具有腐蚀且不能用强碱中和。
这些降解产物逐渐积累将会是溶液起泡,同时也增加了设备的腐蚀。为了回收和净化乙醇胺溶液,有的流程中设置了釜式蒸馏、净化溶液。其原理是加强碱或纯碱在加热的条件下使其和胺类所生成的酸性盐在进化釜里产生热分解,则乙醇胺被游离出来。
3.5脱硫的开、停车及正常操作
3.5.1乙醇胺溶液脱硫的开车
乙醇胺溶液脱硫装置首次开车要进行设备的清洗,洗去油污和锈垢等,使其循环的乙醇胺溶液不被外来的脏物所污染。先用冷水进行清洗,然后再用热的溶液进行彻底清洗。洗液可以用磷酸钠溶液等,一般磷酸钠溶液配成3%-5%(质量浓度)。清洗前系统用氮气置换,使氧含量小于0.5%,然后吸收塔用氮气充几千克压力,具备溶液在系统循环所需的压力。将洗液用泵打入循环清洗。循环24小时后将洗液拍点,多次用软水进行彻底清洗,取水样做消泡实验,直到合格,否则用洗液重新清洗。
乙醇胺系统开车时,先将循环泵开启来,在开泵前注意排掉泵体管道内的气体。调好循环量,溶液的循环量与进吸收塔的天然气量成比例。送低压蒸汽入再沸器,注意暖管,排掉冷凝液,避免发生水锤。将溶液升温到再生塔的正常操作温度,然后再向吸收塔缓慢送气。稳定一段时间后析出吸收塔天然气硫含量,合格后送至下一工序。如果乙醇胺脱硫系统需要停车则首先切断天然气,停止向吸收塔送气,系统的溶液继续循环再生,逐渐减再沸器的蒸汽,直到全停,待再生塔底溶液温度降至65℃以下再停循环泵。如本系统不需要检修,则溶液可以不必排出,用天然气或氮气保压,如需检修,则将溶液排入储槽,用氮气或天然气保压,使氧不漏入系统。
3.5.2保证乙醇胺溶液脱硫的正常操作
A.控制好再生的温度、压力,使溶液再生完全。
B.保证溶液的浓度。低了要补加新溶液;注意控制塔的液位;因溶液在使用过程中所损失,要经常补加软水货乙醇胺溶液。
C.保证循环系统的正常运转,要经常检查泵体、电机。
D.加强溶液的维护。在流程中溶液进行部分过滤,过滤了部分溶液就可使乙醇胺溶液能够正常操作,不致产生泡沫,在运转中应注意过滤器的清洗。
E.控制好乙醇胺溶液的循环量。乙醇胺溶液的循环量是根据天然气里的硫含量来定的,在正常运转中如果循环量低了,将影响脱硫效果。在操作中要注意防止天然气中夹带的凝析油,因凝析油带入吸收塔后,会严重污染乙醇胺溶液,使溶液起泡,造成吸收塔液泛。
3.6胺法的一般操作问题
3.6.1胺法存在的一般操作问题
A.设备腐蚀
醇胺法装置存在的腐蚀:电化学腐蚀、化学腐蚀和应力腐蚀。
a.主要的腐蚀剂是酸性组分(H2S、CO2)本身。游离或化合的CO2在高温和水存在时腐蚀更严重。
b.次类腐蚀剂是溶剂的降解产物
它们在装置的受热部分会如螯合剂一样和铁作用促进设备腐蚀。
醇胺与原料气中的CO2或有机硫发生副反应,最终生成N-(2-羟乙基)-乙二胺。
c.悬浮固体颗粒对设备的磨蚀
溶液中悬浮固体颗粒为FeS。在换热器管子和管路中的高速流动,都会因加速FeS膜的脱落而加快设备腐蚀。
C.垢污改变流道引起的冲刷
结垢物的生成会改变流体的流道形状,使管子沿流道形状出现冲刷。
d.应力腐蚀
由醇胺、H2S、CO2和设备残余应力共同作用下发生的,特别是高温部分尤易发生。
B.溶液发泡
易引起溶液发泡的杂质有:醇胺的降解产物;溶液中的悬浮的固体(如腐蚀产物硫化铁);原料气带入装置的烃类凝液或气田水;进入溶液的外来物质。溶液发泡会使处理量大幅度下降,这样甚至要停车处理;发泡也会造成溶剂损失量增大;同时溶液脱硫效率要受影响。
C.醇胺溶剂的损失
a.溶液蒸发损失
T、P和胺浓度会影响胺蒸发损失量。T增加或P减少则胺的蒸发损失增加。 b.气相夹带
吸收塔塔顶气体的夹带(较大)、闪蒸罐的闪蒸气的夹带(较少)、汽提塔塔顶气体的夹带等(较少)。
c.溶液降解
分为热降解、氧化降解和化学降解三种,造成溶剂损失的主要为化学降解。 d.溶液中非酸气的夹带
e.胺液在烃液中的溶解
当T增加或P降低,液烃携带的胺液量增加。
D.溶液中非酸气的夹带
在高P下脱酸气时,溶液中非酸气的夹带量增加。
3.6.2操作要点
A.保持溶液清洁
为防止各种杂质进入溶液,尽量除去杂质或降解产物,方法有:原料气分离;溶液过滤;溶剂复活;控制溶液发泡(或加消泡剂)。
B.加强防腐措施
加强防腐措施有:合理的设计、溶液过滤和复活;避免氧进入装置;正确的开工、停工操作;合理的酸气负荷;使用缓蚀剂;再沸器中溶液T与所有蒸汽T应尽可能低;除去悬浮固体与分解产物;避免用高温热载体,使金属壁面的温度较低。
C.补充水分
因出吸收塔净化气、出再生塔酸气及闪蒸气会带走胺液中的水分,所以要补充一定的水分。补充水分的方法有:回流一起打入汽提塔内;打入吸收塔顶的水洗塔板上。
D.降低操作成本
降低操作成本的方式有:合理地控制再生温度和回流比;加强闪蒸;回收能量。
3.7选择性脱硫工艺的发展
主要体现在脱硫溶剂的发展上:
A.以MDEA水溶液为主体,加人少量添加剂进一步提高选吸效果;
B.把MDEA和物理溶剂相结合,以提高溶液的硫负荷和改善其脱除有机硫化物的效果;
C.从分子设计的概念出发,合成了选吸性能比MDEA更好的空间位阻胺脱硫溶剂;
D.对选择性吸收过程的反应机理已有较明确的认识,形成了较完善的数学模型和相应的计算软件。
4 节能
4.1装置能耗
装置中主要的能量消耗是在闪蒸罐、换热器和再生塔。
4.2节能措施
由于天然气工业上需要进行脱硫脱碳处理的原料气情况十分复杂,单一的醇胺脱硫脱碳技术不可能解决所有的问题。醇胺脱硫脱碳工艺已由使用单一醇胺溶液发展到经不同溶剂复配成的系列配方脱硫脱碳溶剂,从而实现溶剂操作性能的提升和应用范围的拓展以针对性地解决生产实际问题。实际应用表明,系列配方型脱硫脱碳溶剂的推广应用对天然气净化装置起到了节能降耗、减少生产成本、增加装置处理量等明显效果。
物理溶剂或物理化学溶剂具有有机硫脱除率高、能耗低等优势,尤其是在需要大量脱除有机硫的场合,此类方法具有独特的优越性。特别是在高压下使用时,可以通过多级闪蒸实现对物理溶剂的再生,节能效果明显。采用吗啉衍生物作吸收溶剂的Morphysorb工艺就是近年来新出现的物理溶剂脱硫脱碳技术,具有良好的有机硫脱除能力。其工业试验也颇具特色,是通过从原料气中脱除部分酸性组分提高下游天然气净化厂的处理能力,所得酸气直接注入地层,不建硫磺回收装置。这对消除现有装置
MDEA天然气脱硫工艺流程67_脱硫工艺
处理能力“瓶颈”问题是一个可行的选择。
5 环境保护
5.1建设地区的环境现状
仪陇县介于北纬30°11'—31°39',东经106°14'—106°52'之间,位于四川盆地北部低山与川中丘陵过渡地带。全县总土地面积169170公顷,其中耕地43275公顷,人均耕地0.048公顷。境内山峦起伏,沟壑纵横,地势复杂。地貌以低山梁丘为主,山体切割较深,海拨高差309-793米。
动植物资源:仪陇县位于四川盆地东北部低山与川中丘陵过渡地带,幅员面积1,691km2,境内土地肥沃,气候适宜,雨量充沛,动植物资源非常丰富。粮食作物主要有:水稻、小麦、玉米、薯类、豆类;经济作物主要有:棉花、油菜、花生、药材、黄红麻等;森林资源主要有:柏树、马尾松、香樟、桉树、千丈、桤木、杨槐、马桑、黄荆等乔、灌木;经济林木主要有:柑桔、苹果、梨、核桃、板栗、桃、李、杏、黄连、杜仲等;国家珍贵树种红豆树在仪陇也有少量生长。1998年全县森林覆盖率达到30.1%。
水力及水产品资源:广阔的水域,丰富的水产品资源。县境内有嘉陵江、仪陇河、绿水河、消水河等“一江三河”,加上思德水库、百胜水库等星罗棋布的大小水利设施,全县水域面积达10,000公顷以上,给淡水养鱼提供了有利条件,鲤、鲫、草、鲢四大家族均宜生长;二道河的龙虾肉质细嫩,营养丰富,远近闻名。全县水能装机总容量43,730千瓦,除嘉陵江林家壕电站未开发外,已开发3,730千瓦。
5.2、主要污染源和污染物
SO2废气、COD废水、废催化剂、清管废渣、噪声等。
5.3、污染控制
近年来,为了提高硫磺收率以保护环境、为解决从贫酸气及组成复杂的原料气中
回收硫磺等棘手问题,克劳斯硫磺回收及尾气处理工艺出现了许多新进展。目前主要的技术发展动向大致包括以下四个方面:
(1) 从促进克劳斯反应平衡的角度出发,提高反应转化率; (2) 充分利用各种工艺类型优势,对各种工艺类型进行组合; (3) 采用新型催化剂,达到提高转化率或节能降耗的目的;
(4) 采用新型设备,通过改变操作参数,达到提高装置效能或节能降耗的目的。 为使仪陇天然气处理厂废气、含COD废水、废催化剂、清管废渣、噪声等能够满足国家相关法律法规要求,本工程拟采取以下环保措施:
气田开发拟采取的措施为:①钻井废水和气田采出水全部采用回注地层的方式处理,不外排;②测试、放喷的天然气经点燃后排放,将H2S转化为SO2,降低了毒害性;③钻井废渣采用固化后无害化填埋;④尽量选用低噪声设备,采用相应的隔声、减噪和减振措施。
净化厂拟采取的措施为:①采用SCOT尾气处理装置,尾气焚烧炉排出的尾气由120m高烟囱排放;②污水拟采用SBR处理后进行达标排放;③废催化剂送有处理资质的单位处理或送催化剂生产厂家回收利用;④尽量选用低噪声设备,采取相应的隔声、减振和降噪措施。
集输工程拟采取的措施为:①施工期生态补偿和迹地恢复措施;②项目营运过程中清管作业、场站检修或事故性放空时,放空的天然气通过放空火炬燃烧后排放,为了保证及时点火燃烧,放空火炬配备了灵敏的自动点火装置;③废水为站场值班人员生活污水,生活污水清污分流,粪便采用旱厕收集后用作农业灌溉,洗涤污水用于站内绿化灌溉;④输气管道采用埋地敷设,在正常生产过程中不会产生噪声污染;站场尽量选用低噪声设备,采取相应的隔声、减振和降噪措施;⑤固体废弃物主要为清管作业的废渣、检修时的废渣、值班人员的生活垃圾。清管废渣、检修废渣选择合适的地点无害化填埋;生活垃圾定点收集,定点处理。
6 物料衡算与热量衡算
本设计采用45%的MDEA水溶液作吸收剂。
6.1天然气的处理量
原料气处理量为:3.43×105m3/d。温度为30℃。压力位2.2Mpa(表压)。 查得天然气及其组分有关性质如表:
Tc=?yiTic?194.134K Pc=?yiPic?4.696MPa
则
194.132.2
Pr???0.468
Pr4.696
Tr?
TTcP
?
303.15
?1.56
查《天然气利用手册》图4-5得压缩因子Z?0.998 每小时天然气的处理量为:
n?
PVZRTt
?
?2200?101.325??343000
0.998?8.314?303.15?24
?1.308?10kmol/h?3.631kmol/S
4
气体吸收过程中非酸性组分假设不被吸收,则其摩尔流量为
G?n?(1?yH2S?yCO2)?3.631?0.9738?3.535kmol/s
6.2 MDEA的循环量
由于MDEA 对CO2选择性吸收,吸收因子为2-3.5,这里取为3.2 由 ??
?H
2S
?CO
2S
0.99933.2
2
得 ?CO?
2
?H?
??0.3123
故脱除的H2S的摩尔分数为:0.02050?0.9993?0.020486 脱除CO2的摩尔分数为:0.00570?0.3123?0.00178
脱除酸气的量为:3.535?(0.020486?0.00178)?0.08086kmol/s=291.0 kmol/h
MDEA的酸气负荷由《天然气利用手册》和《天然气加工工程》可查得在0.5以上,在这里取0.5kmol酸气/kmolMDEA,同时由《天然气利用手册》查得再生后的MDEA溶液的酸负载为 0.003mol/mol。45%MDEA溶液的摩尔浓度为
CM?3.882kmol/m,那么解吸后的再生溶液酸含量x2?0.01165kmol/m。
3
3
单位时间内H2S的处理量为G?y1??s?3.535?0.02107?0.9993?0.07441kmol/s 胺的循环量
V?
G?y1??sq?CM
?
3.355?0.02107?0.9993
0.5?3.882
?0.03832m/s?2.299m/min
3
3
为了保证运行安全和达到处理要求,胺的循环量需留有一定的安全欲度,这里取2.400m/min
3
其中:
G—原料气惰性组分流量,kmol/s Ma—醇胺化合物相对分子质量 q—MDEA的酸气负荷, mol/mol 物料恒算
原料气含量y1?
0.020500.9731
?0.02107
y2?20mg/m3?1.42?10?5 由吸收物料守恒:G(y1?y2)?L(x1?x2) 可得:x1?1.677kmol/m3
表6-1物料衡算
G—原料气惰性组分流量,kmol/s
L—胺循环量,m3/s
y1 y2 x1 x2
3.535 0.04 0.02107 1.42*10^-5 1.677 0.01165 0.9993 0.3123
?H
2S
?CO
2
热量恒算
脱除的CO2和H2S量分别为:
3.631?0.0205?0.9993?60?34.076?152.1kg/min3.631?0.0057?0.3123?60?44.01?17.07kg/min
根据文献数据,取CO2与MDEA的反应热为-1420kJ/kg,H2S与MDEA的反应热为-1050kJ/kg。因而酸性气体与醇胺反应放出的总热量为:
17.07?1420+152.1?1050=183944.4kJ/min
近似认为净化气为甲烷(相对分子质量为16),离开吸收塔净化器温度与贫液进塔温度相同,
MDEA天然气脱硫工艺流程67_脱硫工艺
即为40℃。查基础数据可得:甲烷比热容为1.545kJ/(m3?K)
净化气体带出的热量为: 1.545?
343?10?0.95381
24?60
3
?(40?30)?3510.1kJ/min
由《天然气加工工程》公式CP?3.3536?0.00435T
在40℃时45%的MDEA溶液的比热容为CP?3.3536?0.00435?40?3.528kJ/(kg?K) 不考虑吸收塔热损失,则MDEA溶液经过吸收塔的温升为
183944.4?3510.12.4?1028?3.528
?20.73K
富液温度远高于贫液温度,假设不正确,所以在吸收过程中应设置冷凝装置,保证贫富液温度相差不大。
假设富液温度为45℃,冷凝装置的热负荷为
183944?.4
20.73
3510.1?15.7?3
1369kJ14.2
/min
吸收塔出口富液与再生塔贫液进行二次换热,使富液温度达到65℃,进入闪蒸罐,闪蒸出重烃组分。可由《天然气利用手册》假设经过贫富液第一级换热器使富液温度达到80℃,贫液温度将为90℃,富液进入再生塔进行溶剂再生。
设再生塔塔顶温度为105℃,塔底温度为110℃,再沸器温度118℃,回流比R=2:1。 ⑴再沸器热量恒算: ①贫液温升带走的热量:
Q1?2.4?1028?3.528?(110?85)?217607.04kJ/min
②塔顶酸气热负荷
Q2?(152.1?17.07)?1.403??100-85??3560.7kJ/min
③酸性组分解吸热
Q3?183944.4kJ/min
④回流热
Q4?(152.1?17.07)?4.2?2??85-45??56850.5kJ/min
所以再沸器的热负荷为
4
Q沸?
?Q
i?1
i
Q沸?217607.04?3560.7?183944.4?56850.5?461962.6kJ/min
塔顶冷凝器热负荷
Q2?(152.1?17.07)?(4.2?2?1.403)??100-45??91189.4kJ/min
⑵一级换热器热量衡算
热量衡算公式Q?K?A??tm?qm1?cp1??T1?T2?
?tm=
?T1?t1???T2?t2?
T?t?11?ln
?T2?t2?
贫液温度: T1=110℃,T2=90℃, 富液温度: t1=85℃, t2=65℃
?tm=?T1?t1?=?T2?t2?=25℃
采用管壳式换热器,热物流走管程冷物流走壳程,由45%MDEA溶液的粘度公式
lg???3.6587?
1326T
贫液粘度:?1?0.9833mPa?s 富液粘度:?2?1.412mPa?s
由已知粘度范围查《化工单元设备设计手册》取传热系数K?175w/?m2?k?
qm1?cp1??T1?T2?
K??tm
2
?A??0.7450m
留有一定欲度可取实际换热面积为A?0.9m
⑶二级换热器热量衡算(与一级换热器计算方法相同) 贫液温度: T1=90℃,T2=70℃, 富液温度: t1=65℃, t2=45℃
?A?1.3m
2
2
表6-2热量衡算
设备
吸收塔冷凝装置 再沸器
解吸塔顶冷凝器 一级换热器 二级换热器
热负荷kJ/min 136914.2 461962.6 91189.4
换热面积/㎡
0.9 1.3
7.天然气脱硫工艺主要设备的计算
天然气脱硫工艺主要设备的计算主要包括塔设备、分离器、换热器以及再沸器的计算。
7.1MDEA吸收塔的工艺设计
7.1.1选型
根据《气田天然气净化厂设计规范》可知,浮阀塔盘具有弹性大、效率高、处理能力比泡罩塔和筛板塔的特点,故吸收塔、再生塔宜优先采用浮阀塔。因此,在本次设计中优先采用浮阀塔。
在计算塔径时,考虑到胺液易发泡的特点,不宜采用过小的板间距,并考虑原料量处理的大小和塔径大小,板间距选为450mm,为检修方便有人孔处板间距为700mm。
7.1.2塔板数
如前所述,MDEA对H2S、CO2的吸收为化学吸收。吸收过程中放出的反应热是随塔板数变化而变化的。MDEA为叔胺,其与H2S及CO2的反应机理如下:
???(RNH)S2R3N?H2S???2
???2RNHHS(RNH)2S?H2S???3
???(RNH)CO 2R3N?H2O?CO2???23
???2RNHHCO (RNH)2CO3?H2O?CO2???33
根据《天然气加工工程》知,对于胺溶液的吸收塔一般取4-5个理论板,塔板效率均为25%-40%。
取理论板数Ne=5;塔板效率?=25% 则实际塔板数为:Np=5/0.25=20
此塔板数可将净化气中H2S的含量降至20mg/m3以下。
7.1.3塔径
307?10m/d
3
3
的天然气在30℃,2200KPa下的流量为:
?3.5532m/s
3
Vs?
307?10
3
24?3600
液体循环量Ls为MDEA的循环量,由上部分计算得知Ls=0.04m3/s。 天然气相对分子质量为Mg??yiMic?16.836g/mol 天然气密度?g?
PMgZRT
0.5
?
?2200+101.325??16.836
0.998?8.314?303.15
0.5
?15.403kg/m
3
FLV
?Ls???l?????????Vs???g??
?0.04??1028.0?
???????3.5532??15.403?
?0.09197
塔板间距为:HT?450mm
查阅《石油化学工程基础》液层高度hL介于0.05—0.1m,取hL?60mm
由图可查得C20?0.078 ∵液相45%MDEA的表面张力
?L?55.65?0.1376T?55.65?0.1376?30?51.5232mN/m?20mN/m
∴查得结果C20按下式校正 ???
C?C20?L?
?20?
0.2
?51.5232?
?0.078???
20??
0.2
?0.09425
最大允许气速:
umax?C?
?0.09425?
?0.7642m/s
∵MDEA不易发泡,取泛点百分率为0.85 实际气速:
u?0.85umax?0.64957m/s
塔径:
D?
?
?2.64m
MDEA天然气脱硫工艺流程67_脱硫工艺
按《气田天然气净化厂设计规范》的标准,将塔径圆整为3m。
7.1.4堰及降液管
采用浮阀塔板,由《常用化工单元设备的设计》,因塔径为3m,在2.0m以上,所以采用双流型,选定:
直径D?3000mm?3m 塔截面积AT??
D?7.065m
22
板间距HT?450mm 管宽Wd?240mm Ad/AT?9.8% LW/D?0.589 降液管面积Af?0.098?7.065?0.6924m2 堰长Lw?0.5890D?1.767m 若为平堰,堰上清液层高度:
2
h?0.00284E??Lh?3
ow
?L?
w?
其中:L3h液流量,Lh?m/min?144m3/h
Lw?1.767m
E:液流收缩系数,取E=1.08
2
h0.00284?1.08??144??3
ow?1.767??0.05765m(平堰)
??
因为how>6mm,所以不能采用平堰 故应缩短堰长或改用齿形堰 另取
LwD
?0.55,Lw?0.55D?1.65m
由上图得E=1.09
h/3
ow?2.84?1.09?(
1441.65
)
2?0.06005m?6mm
验证正确。 综上堰高:
hw?hL?how?60?6?54mm
第- 36 -页
4
7.1.5浮阀计算
(1)选用重33g的F1型浮阀,其孔径为d0?39mm,取阀孔动能因子F0?9 (2
)由F0?u0
则可得气速u0?故每层塔板上的浮阀个数为:
N?
Vs
0.785?d0?u0
2
?
?2.293m/s
?
3.5532
0.785??0.039??2.293
2
?1297.8,取N=1298
(3)浮阀排列采用等边三角形叉排。 鼓泡区面积:
Aa?
12
tsin60
12
2
,取孔间距t=75mm,
2
?3
2
则:Aa?
?0.075sin60?2.44?10m
12?
?4
开孔总面积A0?
?
4
d0?
2
12
?
?
4
?0.039?5.97?10
2
m
2
所以,作等边三角形排列的阀孔中心距为:
t?d?0.039?
?75mm
符合标准孔间距(GB1118) 故:有效传质区的开孔率为 ??
A0Aa
?100%?
5.97?102.4?10
?4
?3
?23.73%
7.1.6 塔板压降
hf?hd?hl
其中:hf:气象通过塔板的压降
hdhl
:干板压降 :液层阻力
浮阀塔hd的计算公式
第- 37 -页
阀孔全开前hd?19.9
uo
0.175
?l
uo?v2g?l
2
阀孔全开后hd?5.34
联立上两式求临界孔速uoc,即19.9?2g?uoc0.175?5.34?vuoc2 解得uoc?2.3777m/s 又阀孔速度uo?
USAU
?
3.55325.97?10
?4
?1298
?4.585m/s
故:uoc<uo,既浮阀全开. 则,hd?5.34
uo?v2g?l
2
?0.0253m
hl?0.5(hw?how)?0.5(0.054?0.06005)?0.05703 所以有:hf?hd?hl?0.0253?0.05703?0.08233m 液体在降液管内停留时间的核算 ①液体在降液管内实际停留时间?' ?'?
Af?Hd
LS
又hd?hw?how?hf?hof??, 其中:hw=0.054m
how=0.06005m hf
=0.08233m
?为板上液面落差,对浮阀塔而言?很小,一般可忽略。
hof
?LS?
?0.153??
L?ho??w
2
取降液管端部与塔板的间隙高度ho=0.04m
第- 38 -页
hof
0.04??
?0.153??0.0562m ?
?1.65?0.04?
2
hd?0.054?0.06005?0.08233?0.0562?0.2526m
0.6924?0.45
0.04
?7.7895s?(3~5)s
②液体在降液管内的最大停留时间?? 综上计算符合,可行。
Ad?HT
LS
?
7.1.7塔附件设计
①接管直径
a. 原料天然气进料口大小
已知气相流量为3.5532m3/s,取管内流速为30m/s
D?
?
?0.3884m
查标准系列选取DN400
b.湿净化天然气出口 查标准系列选取DN400
c.MEDA输送管线,取MEDA流速为0.5m/s ②除沫器
由工艺条件知需设置除沫器,以减少液体夹带损失,确保气体纯度,保证后续设备的正常操作。本设计采用丝网除沫器,其具有比表面积大、质量轻、空隙大及使用方便等优点。
设计气速选取:u?kk'?0.107
故u?0.107?
?0.8676m/s
除沫器直径D?
?
?2.284m
选取不绣钢除沫器,类型:标准型;规格40-100;材料:不绣钢丝网;丝网尺寸:圆丝?0.60。
第- 39 -页
③封头
封头分为椭圆形封头、蝶形封头等几种,本设计采用椭圆形封头,由公称直径
DN?3000mm,查得总深度H?790mm
,内表面积A?10.1329m2,容积V?3.170m3。
④裙座
塔底常用裙座支撑,裙座的结构性能好,连接处产生的局部阻力小,所以它是塔设备的主要支座形式,为了制作方便,一般采用圆筒型。
由于裙座内径?800mm,故裙座壁厚取16mm。
基础环内径:Dbi??800?2?16???0.2~0.4??400?752mm 基础环外径:Dbo??800?2?16???0.2~0.4??400?912mm 圆整得:Dbi?800mm,Dbo?1000mm 对于基础环厚度,考虑到腐蚀余量取18mm 裙座高度取2m,地脚螺栓直径取M32 ⑤人孔
人孔是安装或检修人员进出塔的唯一通道,人孔的设置应便于进入任何一层塔板,由于设置人孔出塔间距离大,且人孔设备过多会使过多制造时塔体的弯曲度难以达到要求,由《气田天然气净化厂设计规范》知,对D?800mm的吸收塔为安装检修的需要,一般每隔4~6层塔设一人孔,人孔直径一般为400~500mm。
故本文拟定每7层设一人孔,选用D
g
450的人孔,共4个。分别设在第1、8、15
层塔板上和20层塔板下。每个人孔直径为450mm。在设置人孔处,板间距为700mm,裙座上应开2个人孔,直径为450mm,人孔伸入塔径应与塔内壁修平,其边缘需倒棱和磨圆。人孔法兰的密封面形状及垫片用材,一般与塔德接管法兰相同,本设计也是如此。
7.1.8塔体总高度的设计
塔总高度(不含塔裙座)由下式决定:
H?HD?(N?2?s)HT?S?HT'?HF?HBHD:塔顶高度,m. 取HD=1.8m
第- 40 -页
MDEA天然气脱硫工艺流程67_脱硫工艺
HT
:踏板间距,m. 取HT=0.45m
HT':开有人孔的塔板间距.HT'=800mm=0.8m HFHB
:进料段高度(吸收塔,从塔底进料), H:塔底空间,取H=3m
B
F
可忽略.
N:实际塔板数,N=20.
S:人孔数目(不包括塔顶空间和塔底空间的人孔数),取S=4. 综上:
H?1.8?(20?2?4)?0.45?4?0.8?3?14.3m
7.2解吸塔
7.2.1 计算依据
1.入塔胺液流量;
2.出塔酸气的组成和流量见前面物料衡算;
3.塔底贫液流量和组成与吸收塔的进料胺液相同; 4.操作压力180Kpa;
5.入塔富液的温度85℃,出塔贫液温度110℃;
6.由于浮阀塔的结构简单,制造方便,价格低;塔板开孔率大,生产能力大,操作弹性大,塔板效率较高等优点,故吸收塔采用浮阀塔。
7.2.2塔板数的确定
1.根据以有的经验数据选取4块理论塔板数;
2.板效率为25%~40%,设计中选用30%。则:实际有效塔板数为: 4÷0.3=13.3块 圆整为14块。
3.为了降低胺液的蒸发损失应该在进料上部有2~6层板。考虑MDEA的蒸发损失较小所以3块。所以解吸塔的实际塔板数为:14?3?17块
7.2.3解吸塔的工艺条件及有关物性的计算
1.操作压力:180Kpa;
2.操作温度:塔顶85℃,塔底110℃;全塔由反应热全塔的平均温度按胺液计算得:97.5℃ 3.平均摩尔质量的计算 塔顶气体流量为: H2S 136.1kg6
n/mi
/mi n
CO2 15.28kg
回流比??2
则水的流量为:?136.16?15.28??2?302.88kg/min
n
M?
?
i?1
XiMi
表7-1解吸塔塔顶气体平均摩尔质量 组分
质量流量kg/min
Mi
H2S CO2
136.16 15.28 302.88 454.32
34.082 44.01 18
水 总计
塔顶气体平均摩尔质量:MVDM?21.46Kg 由于MDEA的沸点大,塔底气相组成大部分为水:
∴塔底气体平均摩尔质量为:MVWM?19KgKmol 全塔气体平均摩尔质量:MVM? 4.平均密度 塔中气相平均密度: ?VM?
22.4?
M
vm
21.46?19
2
?20.23KgKmol
273.15?t273.15
?
0.1013P
?
20.23
273?97.5
22.4??
273.15
?15.11Kgm0.10132.3
3
对于胺液的平均密度:
?AM?1.0991?0.000223T?0.000001425T
2
?g
cm
3
?
2
?1.0991?0.000223??273.15?97.5??0.000001425??273.15?97.5?
?0.986?gcm3??986Kgm3 5.液体平均表面张力
由45%MDEA的表面张力计算公式:
??55.65 .?0.13?7t6??55.6?0.137?697
?42.1d8yn?
42.m1 m
7.2.4解吸塔的塔体工艺尺寸计算
1.塔径的计算
吸收塔采用浮阀塔板式塔,吸收塔的最大空塔气速由公式:
????v?
2?l ?max?0.076??
?v??
0.5
0.5
?986?15.1?1
得: ?max?0.076?2???
15.11??
0.61m0s
为了防止液泛和允许溶液起泡,气速应分别降低为75%~25%,和25%然后在由降低的气速计算塔径。
?max?0.?70.61?08 根据MEDA物性,取 ??0.7
0.m4s8
塔径
:D?
(6-7)
此时Vs在操作条件下(97.5℃,0.18Kpa)时的气体体积,由状态方程: VS?V0?
T1T0
?P0P1
V0=22.46?22.4?3600?0.14m3s
VS?0.14?
273.15?97.5
273.15
?0.10130.18
?0.11m/s
3
?0.572m
将Vs带入上式(6-7
)D?按照标准塔径圆整为:D=1m
塔的横截面积为:AT?
?
4
?
D?
2
?
4
?1?0.785m
22
实际空塔气速为:??
VsAT
?
0.110.785
?0.14ms
2.解吸塔有效塔高的计算
取板间距为0.35m,在塔底,第9块板及塔顶分别开一入孔(3个入孔),取其间距为0.6m,
顶部塔板与捕雾器的间距取1m。 故解吸塔的高度为:Z?(17?3)?0.35?2?0.6?1?6.1m
8参数校核
8.1浮阀塔的流体力学校核
8.1.1溢流液泛的校核
因Fo?u0?4.585?17.99??5,6? 故不会发生漏液,不用校核。
8.1.2液泛校核
降液管到下塔板间距:
h0?0.04m
液体通过降液管底部的阻力:
?LS?0.04??
hd?0.153???0.153?????0.0562m
?1.65?0.04??Lw?h0?hp?
hfg?l
?
0.082339.81?1.028
?8.16?10m
?3
2
2
液柱
Hd?hp?hl?h
d
?8.16?60?56.2?124.36mm
为防止液泛现象发生应使:
?Hd?
H?h?w?T?
???
一般取??0.5,但由于发泡严重的物质一般取较小值,故在这里取??0.5。
校核:450?54?504?
124.360.5
?248.72
所以符合要求,不会发生液泛现象。
8.1.3液沫夹带校核
un0.0057?
由ev??
?l?HT?2.5hL
??'?
3.2
其中:
?:液相表面张力,前面也算。?=51.5232mN/m
un:气速un?
UsAT?Af
3
?
3.55327.065?0.6924
?0.5576m
HT
=0.45 m/s
hL':板上液层高度.hL'?hw?how?0.054?0.006?0.06m
综上:
0.5576??
ev????
51.5232?0.45?2.5?0.06?
5.7?10
?3
3.2
?8.04?10
?4
?0.1
故液沫夹带量ev在允许范围内。
8.2塔板负荷性能计算
8.2.1漏液线(气相负荷下限线)
以F0?
6作为气相最小负荷的标准。则由F0?
u得u0?
2
,故:
Vs,min?0.785d0N
2
?0.785?0.039?1298?
2
?2.369m/s
8.2.2 过量雾沫夹带线
以eV?0.1kg液/kg气为标准,根据前面雾沫夹带校核可知,对于大塔,取泛点率F = 0.8,求V与L的关系。
MDEA天然气脱硫工艺流程67_脱硫工艺
由F?
AaKCF
?
8.484?0.85?0.14
?0.122V?0.884L?0.8
得:V?6.556?7.246L
8.2.3 液相负荷下限
由于堰上液层高度how较小,会使堰上的液体分布不均匀,影响传质效果,设计时应大于6mm,对于平直堰,取堰上液层高度h作为最小液体负荷标准。 ?0.006mow
取E?1.0 由hOW?0.00284E(
3
LlW
)
2/3
?0.00284?1?(
L1.767
)
2/3
?0.006
得:
Lmin?5.426m/h?0.00151m/s
3
8.2.4 液相负荷上限
液体的最大流量应保证在降液管中停留时间不低于3~5s,取??5s作为液体在降液管中停留时间的下限,则:
由??
AfHT
L
?
0.6924?0.45
L
s /
?5得:
3 Lmax?0.062m3
8.2.5 液泛线
为防止发生液泛现象,应满令 Hd??(HT?hw) 由 联立得:忽略
aV
2
Hd??(HT?hW)
。
Hd?hp?hL?hd
;
hp?hc?h1?h?
;h1??hL;hL?hw?how
?HT?(????1)hw?(??1)how?hc?hd?h?
h0W
h?
,将与L,
2/3
hd
与L,
hc
与V的关系式代入上式得:
?b?cL?dL
2
式中:
a?1.91?10
5
?V?L?n
2
?1.91?10?
5
15.111028?1298
2
?0.00167
b??HT?(????1)hW?0.5?0.45?(0.5?0.5?1)?0.044?0.1810
c?
0.153(lWh0)
2
?
0.153(1.767?0.04)
1lW
2/3
2
?30.627
11.767
2/3
d?0.667(1??)E?0.667?(1?0.5)?1.08??0.74
222/3
故 : 0.00167V?0.1810?30.627L?0.74L
P?2200kpa V?20?103m3/d 由HYSYS软件模拟工艺流程的结果有: 原料气气体密度:?g?11.21kg/m3 液体密度:?l?995.27kg/m3 质量流量:Ms?3.118kg/s 微粒直径:d0?100?m?10?4m 粘度:?g?1.2132?10?5Pa?s
由《天然气地面工程》书中公式(6—8)计算阿基米德准数Ar
Ar?
d0(?l??g)g?g
3
?g
2
?
10
?4
?(995.27?11.218)?9.81?11.218
(1.2132?10)
?5
2
?735.76
故液体在给定分离条件下出于过渡区 由其利用表(表6—1)中Ar—Re的关系求得
Re?0.153Ar
0.714
?17.043
v0d0?g
由公式(6—9)Re?
Re?gd0?g
?g
得
?5
v0?
?
17.043?1.2132?10
10
?4
?11.218
?0.18432m/s
由HYSYS模拟结果知气体流量为:Q?0.1995m3/s 取L=4D 由公式
L?
4Q0.7?v0D
?D?
?
?0.702m
将分离器长度D圆整为0.8m 分离器长度:L?4D?4?0.8?3.2m 分离效果校核:
He?
4Q0.7?v0D
?
4?0.1995
0.7?3.14?0.8?0.1843
?2.46m
卧式分离器重允许的气体流速为:
vgv?0.7?
D2
2?2.460.8
?0.1843?0.793m/s
h??0.4m
Hevgv
?
2.860.922
?3.10
hv0
?
0.40.1843
?2.17
即
Hevgv
?
hv0
故选卧式分离器可满足分离要求。
10.心得体会
本次工程设计是我第一次独立设计一个化工流程,虽然各种单元操作自信还是学的不错,可是当真正用于实践的时候才发现问题还有很多。首先在选用单元操作的时候只懂得大概应用,可是到具体的设计时工艺参数时就什么都不知道了,虽然通过查阅资料部分解决了这些问题,可是不够理想,其次各个环节单独设计还可以,可是要将这些环节全部串联在一起还是有不少问题,另外虽然能运用CAD画图,但是很多地方和标准规范还是出入很大的,这些都是对设计要求和绘图标准不了解的缘故。但是我也能运用学过的知识解决一些遇到的问题,懂得了理论与实际相结合是很重要的,只有理论知识是远远不够的,只有把所学的理论知识与实践相结合起来,才能提高自己的实际动手能力和独立思考的能力。
为了完成了设计要求,我在图书馆查阅各种书籍,从中找到我们所需要的数据﹑
公式等,但是设计书的前五章,大部分借鉴了往届学长的即成资料,后面部分才是根据自己的处理量完成的。此外我还和几位同学一起商定了此次的设计任务,提出自己想法的时候也吸纳别人的宝贵意见,感谢这些同学们所给与的帮助和支持。
对于这次工程设计我还是要提点建议:一、一个人单独完成一个题目不是很恰
当,每个人都有自己的长处,对相同的设计任务有自己不同的看法,如果多个人完成一个项目的设计,设计结果自然会包含大多数人好的想法,使设计结果更加完善;二、
如果是分组完成的话,不但可以减小单个人的负担,同时分工协作也能让每个人投入更多的注意力于自己的分内之事,真正的在他所处理的那个问题上认识的深一些,我想这样会比单个人只为完成课程任务而机械的计算来的实在一些。三、报告都不是什么特别重要的东西,我觉得应该让大家以上台答辩的形式完成这次工程设计,那样的话,没有真正从事这项工作的人是绝对说不上来的,也是一种促进和监督我们认真学习的好方式,同时也让很多人没有了抄袭的机会。
11.参考文献
1.匡国柱,史启才.化工单元过程及设备课程设计[M].北京:化学工业出版社,2001.10. 2.陈敏恒,方图南,丛德滋,齐鸣斋.化工原理[M].北京:化学工业出版社,2001.
3.谭天恩,麦本熙,丁恵华.化工原理(第二版,上、下册)[M].北京:化学工业出版社,1998. 4.化学工业手册编委合编.《化学工程手册》[M].北京:化学工业出版社,1989.
5.华南工学院化工原理教研组编.《化工过程及设备设计》[M].广州:华南工学院出版社出版,1980. 6.卢焕章.《石油化工基础数据手册》[M].北京:化学工业出版社,1982.
7.天津大学化工原理教研室编.《化工原理课程设计》[M].天津:天津科学技术出版社,1994. 8.徐文源.浅论四川气区高含硫天然气净化及副产品加工利用[J].石油与天然气化工,2001,30(6):278~280.
9.安作相.川东石碳系气藏形成再分析[J].中国海上油气(地质版),1997,11(3):172~177. 10.梁卫,覃建雄.川东石碳系天然气成因类型和气源探讨[J].中国海上油气(地质版),1995,9(2):97~103.
11.原青民。四川盆地高含硫天然气开发中的有关技术问题[J].石油与天然气化工,2002,第31卷增刊:44~47.
12.川东天然气净化总厂.原料气中有机硫的分析报告.内部资料,2002.
MDEA天然气脱硫工艺流程67_脱硫工艺
13.王宏俊等.内蒙古石油化工,1998,24(3):86~87.
14.王荷芳.液化石油气脱硫剂性能研究[D].河北工业大学硕士学位论文,2004.
15.龙晓达.90年代天然气处理加工利用新进展[J].石油与天然气化工,1999,28(4):265~271.
16.于淼,周理.天然气中H2S的脱除方法—发展现状与展望[J].天津化工,2002,(5):18~20.
17.王世娟,王军民.石油气净化脱硫技术的开发与应用[J].化工进展,2002,21(2):140~142.
18.杨敬一.炼厂气选择性脱硫的研究[D].华东理工大学博士学位论文,2002.
19.王瑞,石冈等.工业气体中H2S气体的脱除方法—发展现状与展望[J].天然气工业,1999,19(3):
84~89.
第- 51 -页

五 : AD脱水甘蓝菜工艺流程图
① AD脱水甘蓝菜工艺流程图






61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1