一 : 溶质质量分数分别为a%和5a%的H2SO4溶液按等体积混合,混合溶液中H2SO4的质量分数为()A.
溶质质量分数分别为a%和5a%的H2SO4溶液按等体积混合,混合溶液中H2SO4的质量分数为( )
|
| C |
[思路分析] 本题考查溶液混合后溶质质量分数的变化。设a%、5a%的H2SO4溶液的密度为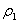 、 、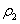 , ,则可知 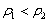 ,所以两种溶液混合后,溶质的质量分数为 ,所以两种溶液混合后,溶质的质量分数为 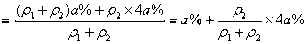 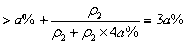 。 。提示: (1)两种不同质量分数的溶液等体积混合,若溶液的密度大于1 g·cm―3,则混合溶液的质量分数大于它们和的一半;若溶液的密度小于1 g·cm―3,则混合溶液的质量分数小于它们和的一半。 (2)无论溶液的密度大于1 g·cm―3,还是小于1 g·cm―3,等质量混合时,混合溶液的质量分数都等于它们和的一半。 |
考点:
考点名称:化学实验的基本操作化学实验的基本操作:
1.药品的取用
(1)药品取用
原则粉状不沾壁,块状防掉底,液体防污染,标签防腐蚀。
(2)固体药品的取用
取用同体药品一般用药匙。有些块状的药品(如钠、钾、磷)可用镊子取用。用过的药匙或镊子要立刻用干净的纸擦拭干净,以备下次使用。往试管里装入同体粉末时,先使试管倾斜,把盛有药品的药匙(如图 A)或用小纸条折叠成的纸槽(如图B)小心地送入试管的底部,然后使试管直立起来,让药品全部落到试管的底部。把块状的药品或密度较大的金属颗粒放入玻璃容器时,应该先把容器横放,把药品或金属颗粒放入容器口以后,再把容器慢慢地竖立起来,使药品或金属颗粒缓慢地滑落到容器的底部,以免打破容器。
(3)液体药品的取用
液体药品通常盛在细口瓶里。取用细口瓶里的液体药品时,先拿下瓶塞,倒放在桌上。然后右手握瓶,使瓶上的标签向着手心(防止残留在瓶口的药液流下来腐蚀标签),左手斜拿试管,使瓶口紧挨着试管口(如右图)将液体慢慢地倒入试管。倒完液体,立即盖紧瓶塞,把瓶子放回原处。
取用一定量的液体药品,可以用量简量出体积。量液体时,量筒必须放平稳,而且使视线与量筒内液体凹液面的最低点保持水平,或者说,视线与量筒内液体凹液面的最低点相切,再读出液体的体积。
滴管是用来吸取或滴加少量试剂的一种仪器。滴管上部是橡胶乳头,下部是细长尖嘴的玻璃管。使用滴管时,用手指捏紧橡胶乳头,赶出滴管中的空气,然后把滴管伸入试剂瓶中,放开手指,试剂被吸入(如 A图)。取出滴管,把它悬空在容器(如烧杯、试管) 上方(不要接触器壁,以免沾污滴管或造成试剂的污染),然后用拇指和食指轻轻挤橡胶乳头,试剂便滴入容器中(如B图)。 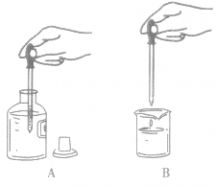
2.仪器的洗涤
(1)洗涤方法
①冲洗法:往容器里注入少量水,振荡,倒掉,反复几次,再使容器口朝下,冲洗外壁后将容器放于指定位置晾干。如果是试管,则应倒扣在试管架上。 ②刷洗法:如果内壁附有不易洗掉的物质,可以往容器里倒入少量水,选择合适的毛刷配合去污粉、洗涤剂,往复转动,轻轻刷洗后用水冲洗几次即可。
③药剂洗涤法:对于用水洗小掉的污物,可根据不同污物的性质用药剂处理。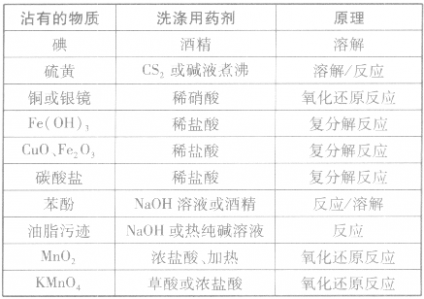
(2)洗净标准内壁上附着均匀的水膜,既不聚成水滴,也不成股流下。
3.试剂的溶解
通常是指固体、液体或气体与液体相混合而形成溶液的过程。
(1)固体:用烧杯、试管溶解,振荡、搅拌、粉碎、升温等可加速溶解.
(2)液体:一般将密度大的溶液注入密度小的溶液中,如稀释浓H2SO4时将浓H2SO4慢慢注入水中。
(3)气体:根据气体溶解度选择水下溶解或水面溶解。 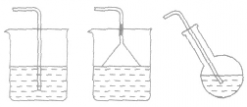
4.物质的加热 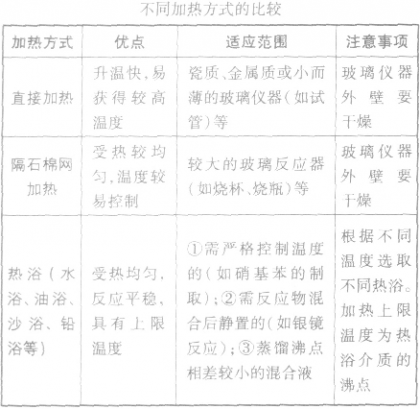
5.仪器的装配和拆卸
装配时,首先要根据装置图选择仪器和零件,然后进行仪器和零件的连接和全套仪器的总装配。
(1)零件的连接
正确连接实验装置是进行化学实验的重要环节。在中学化学实验巾使用较多的是连接玻璃管、橡皮塞、橡胶管的操作。
①把玻璃管插入带孔的橡皮塞
左手拿橡皮塞,右手拿玻璃管。先把要插入塞子的玻璃管的一端用水润湿,然后稍稍用力转动,将它插入。 
②连接玻璃管和橡胶管
左手拿橡胶管,右手拿玻璃管,先把玻璃管管口用水润湿,然后稍稍用力即可把玻璃管插入橡胶管。
③在容器中塞橡皮塞
左手拿容器,右手拿橡皮塞慢慢转动,旋进容器口。切不可把容器放在桌面上再使劲塞进塞子,这样做容易压破容器。 
(2)全套仪器的总装配
一般要遵循“由下而上、由左刮右”的原则。如根据酒精灯高度确定铁架台上铁阁的位置,由铁圈确定圆底烧瓶的位置。又如组装实验室制氯气的装置,先要把氯气发生装置安装好,然后再组装集气装置,最后组装尾气吸收装置。
(3)装置的拆卸
实验结束后要拆卸装置,一般先将连接各部分装置的橡胶管拆开,这样使整套装置分成若干部分,然后再将各部分装置的仪器、零件按“由上到下”的顺序逐一拆卸。
二 : 同时溶解和ICP-AES同时测定铜基锡银焊料中的锡和银
同时溶解和ICP-AES同时测定铜基锡银焊料中的锡和银
摘要:提出了简单、快速地同时溶解及测定铜基锡银焊料中锡银的新方法。合金样品经2 g酒石酸和8mL稀硝酸溶解后。用电感耦合等离子发射光谱仪法(ICP-AES)同时测定溶液中的锡和银。回收率为98%~102%,RSD为0.9%~2.1%.
关键词:铜基锡银焊料;锡;银 ;同时溶解测定 ;电感耦合等离子体发射光谱仪
Simultaneous Dissolution of Tin and Slive in Copper solder andTheir Determinations by ICP-AES
Zheng jianming
Abstract:A new method for the simultaneous dissolution anddetermination of Tin and Silver in copper solder was reported.Thesample was dissolved with 2 g tartaric acid and 8 mL nitricacid,Tin and Silve were simultancously determined by ICP-AES,Therecoveries of the elements were in the range of 98%~102%,and theRSD 0.9%~2.1%.
Key words: Copper solder; Tin; Silver; Simultaneous Dissolution anddetermination;ICP-AES
近年来,锡银合金被广泛应用在焊料行业中,目前对它们的检测项目主要有滴定法和光谱法两种。在该合金分析中,样品中锡银的溶解是分析中最重要的步骤,目前常用的样品溶解方法有:浓硫酸浓硝酸溶解锡银①、王水溶解铜锡②(www.61k.com];③以及稀硝酸溶解锡。这三种方法无论是哪1种都不能同时溶解合金中的锡银。在铜基锡银焊料样品中,含银量都比较高,王水溶解法和浓硫酸浓硝酸法都无法全部能使样品中银溶解,故不能用王水和浓硫酸和浓硝酸处理;而稀硝酸不能溶解锡。基于以上几个原因,我们要检测焊料中的锡银时,样品分解要使用不同的溶解方法,分析过程繁琐。本文研究了使用酒石酸和浓硝酸同时溶解铜锡银合金中的锡和银,最后用电感耦合等离子体发射光谱仪同时测定锡和银④⑤。结果表明:此方法快速,准确。
1 实验部分
1.1 仪器与实验条件
单向观测顺序扫描型电感耦合等立体发射光谱仪(ICP-AES)ICP-2000天瑞仪器股份有限公司生产,仪器工作条件:等离子体线圈功率:1.1KW,高压:4KV,冷却气流量:18L/min,辅助气流量0.5L/min,测定波长:银:328.0,锡235.4。采用径向观测。
1.2试剂
硝酸 优级纯 500 mL /瓶 昆山晶科微电子材料有限公司
酒石酸 分析纯 500 g/瓶 天津大茂化学试剂厂
超纯水 实验室一级用水 南京易普易达设备厂
1.3样品处理
准确称取0.050 g样品于烧杯中,依次加入2.000 g酒石酸,5 mL去离子水和8mL浓硝酸,于100℃加热板上溶解,完全后,冷却,将溶液转移到100 mL 容量瓶中,以水定容,再取10 mL到100mL容量瓶中,稀释10倍待测。
1.4标液配置
分别吸取1000 mg/L银,锡标液0.0、0.1、0.5、1.0 mL至100mL容量瓶中,加入2 g酒石酸以及5mL浓硝酸,去离子水定容.即得0.0、1.0、2.0、5.0、10.0 mg/L的银锡混合溶液。
2结果与讨论
2.1溶解样品试剂用量实验
若溶解锡银,须用硝酸;本研究在固定硝酸用量的情况下,通过改变酒石酸的用量来考察样品溶解效果。实验结果表明:对加入0.0g,0.5g,1.0g,1.5g 四个不同质量的酒石酸的锡银焊料,样品均不能完全溶解,酒石酸的最佳用量在2.0 g。
2.2 试剂加入顺序
实验表明,溶解样品时首先加入酒石酸,将会保证硝酸完全溶解锡而不形成偏锡酸,同时硝酸溶解银。
2.3样品溶解温度及溶解时间的影响
实验表明,溶解温度控制在150℃左右(见图一),同时控制溶解时间(图二),使溶液体积不要由于过多的蒸发引起晶体析出,本实验选用的最佳溶解时间为15min左右。
三 : 一杯酸性的液体
一杯酸性的液体
文/紫竹心
·
几粒果干,几朵腌制的魂灵。
于沸水中悲壮,红色,透过身体。
疼痛早已失忆,翻滚的,不外乎那些思绪。( 文章阅读网:www.61k.com )
酸,只是味觉,掩视涩的心扉。
·
还有什么可以呈现?
文字吗?它们不在其位。
咀嚼剩余的,残渣还在膨胀。
杯中,思想继续。
2016.12.07
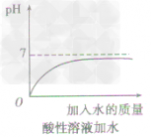
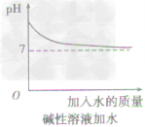
四 : 利用中和反应可以测定酸或碱溶液中溶质的质量分数.例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量
| 利用中和反应可以测定酸或碱溶液中溶质的质量分数.例如,在一定量的待测酸(或 碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数. 右图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图. (1)根据图曲线可以判断实验中是向______(填“酸”或“碱”,下同)溶液(待测液)中滴加______溶液(标准液). (2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到______,则证明中和反应正好完成. (3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计.若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数. 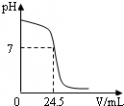 |
| (1)根据溶液的pH变化情况可知,开始时溶液的pH大于7,显碱性,后来溶液的pH小于7,是向碱溶液中滴加酸溶液,故填:碱,酸; (2)酚酞遇碱性溶液变红,遇中性溶液不变色,故填:红色刚好褪去; (3)设待测液溶质的质量分数为x 2NaOH+H2SO4 ═Na2SO4 +2H2O 80 98 25mL×1.0g/mL×x 24.5mL×1.0g/mL×4.5%
x=3.6% 答:待测液溶质的质量分数为3.6%. |
考点:
考点名称:关于溶液的计算溶质质量分数: =
=
 ×100%
×100% 。
。 影响溶质质量分数的因素:
影响溶质质量分数的因素: ×100%
×100% | 方法 | 计算依据 | 计算公式 | |
| 溶液的稀释 | ①加水稀释 ②加稀溶液稀释 | ①加水稀释前后,溶液中溶质的质量不变 ②用稀溶液稀释浓溶液时。稀溶液中溶质的质量与浓溶液中溶质的质量之和等于混合后溶液中溶质的质量 | 加水稀释:稀释前后溶液中溶质的质量不变 m浓×ω浓%=(m浓+m水)×ω稀% |
| 溶液的浓缩 | ①添加溶质 ②蒸发溶剂 ③加入浓溶液 | ①原溶液中的溶质与后加入的溶质质量之和等于混合后溶液中的溶质质量 ②蒸发溶剂前后溶液中溶质的质量不变(没有溶质析出) ③原溶液中的溶质与后加入浓溶液中的溶质质量之和等于混合后溶液中的溶质质量 | 蒸发浓缩:浓缩前后溶液中溶质的质量不变(m稀-m水)×ω浓%=m稀×ω稀% |
 ×100g]可推导出:
×100g]可推导出: ,
,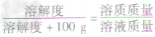
| 溶解度 | 溶质质量分数 | |
| 意义 | 物质溶解性的量度,受外界温度的影响 | 表示溶液中溶质质量的多少,不受外界条件影响 |
| 容积要求 | 100g | 无要求 |
| 温度要求 | 与温度有关 | 一般与温度无关 |
| 溶液是否饱和 | 一定达到饱和 | 不一定饱和 |
| 计算公式 |  ×100g ×100g |  |
| 单位 | 克 | 无单位 |
| 联系 | 饱和溶液中溶质的质量分数= | |
 ×100%
×100% 。
。| 溶液的pH值 | 溶液的酸碱度 |
| <7 | 酸性溶液(pH越小,酸性越强) |
| =7 | 中性溶液 |
| >7 | 碱性溶液(pH越大,碱性越大) |
 pH值测定时的注意事项:
pH值测定时的注意事项:五 : 已知胆矾(化学式为CuSO4·5H2O)溶于水后形成硫酸铜溶液,现将25g胆矾溶于一定量的水(设其质
| 已知胆矾(化学式为CuSO4·5H2O)溶于水后形成硫酸铜溶 液,现将25g胆矾溶于一定量的水(设其质量为m,单位为克)中得到溶质的质量分数为8%的不饱和溶液,则用来完全溶解25g胆矾的水的质量(m)为 |
[ ] |
| A.50g B.75g C.175g D.200g |
| C |
考点:
考点名称:关于溶液的计算溶质质量分数: =
=
 ×100%
×100% 。
。 影响溶质质量分数的因素:
影响溶质质量分数的因素: ×100%
×100% | 方法 | 计算依据 | 计算公式 | |
| 溶液的稀释 | ①加水稀释 ②加稀溶液稀释 | ①加水稀释前后,溶液中溶质的质量不变 ②用稀溶液稀释浓溶液时。稀溶液中溶质的质量与浓溶液中溶质的质量之和等于混合后溶液中溶质的质量 | 加水稀释:稀释前后溶液中溶质的质量不变 m浓×ω浓%=(m浓+m水)×ω稀% |
| 溶液的浓缩 | ①添加溶质 ②蒸发溶剂 ③加入浓溶液 | ①原溶液中的溶质与后加入的溶质质量之和等于混合后溶液中的溶质质量 ②蒸发溶剂前后溶液中溶质的质量不变(没有溶质析出) ③原溶液中的溶质与后加入浓溶液中的溶质质量之和等于混合后溶液中的溶质质量 | 蒸发浓缩:浓缩前后溶液中溶质的质量不变(m稀-m水)×ω浓%=m稀×ω稀% |
 ×100g]可推导出:
×100g]可推导出: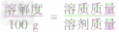 ,
,
| 溶解度 | 溶质质量分数 | |
| 意义 | 物质溶解性的量度,受外界温度的影响 | 表示溶液中溶质质量的多少,不受外界条件影响 |
| 容积要求 | 100g | 无要求 |
| 温度要求 | 与温度有关 | 一般与温度无关 |
| 溶液是否饱和 | 一定达到饱和 | 不一定饱和 |
| 计算公式 |  ×100g ×100g | 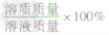 |
| 单位 | 克 | 无单位 |
| 联系 | 饱和溶液中溶质的质量分数= | |
 ×100%
×100% 。
。61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1