一 : 巴豆酸的结构简式为CH3CH=CHCOOH ,现有①水;②溴的四氯化碳溶液;③乙醇;④纯碱溶液;能与之反应的?
巴豆酸的结构简式为CH3CH=CHCOOH ,现有①水;②溴的四氯化碳溶液;③乙醇;④纯碱溶液;能与之反应的?
为什么他能和水反应?
加成,把水分成一个羟基和一个氢原子!

二 : 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOHS
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
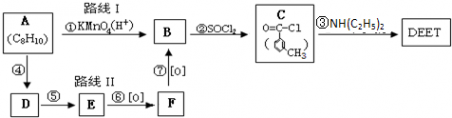 根据以上信息回答下列问题: (1)由避蚊胺的结构简式推测,下列叙述正确的是______. A.它能使酸性高锰酸钾溶液褪色B.它能发生酯化反应 C.它与甲苯互为同系物D.一定条件下,它可与H2发生加成反应 (2)在反应①~⑦中,属于取代反应的有______(填序号). (3)写出下列化学反应方程式:C→DEET______;E→F______. (4)经测定E的同分异构体能与FeCl3溶液发生显色的反应,且结构中不含乙基,试写出符合其条件的任意2个可能的结构简式______. (5)经核磁共振氢谱图显示A的某种同分异构体J只有两个吸收峰(及两种环境的氢原子),试写出J的化学名称______;J物质被酸性高锰酸钾氧化后得到的产物在一定条件下可与乙二醇反应,制成涤纶(聚酯纤维),试写出生产涤纶的化学方程式______. 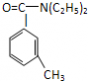 |
由C的结构和题中信息可知A为 ,B为  ,F可氧化为B,则F为 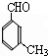 ,E为 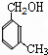 ,则A生成D的反应应为A和氯气发生取代反应生成 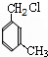 ,  发生水解(或取代)生成  ,则 (1)A.避蚊胺中苯环上含有甲基,与酸性高锰酸钾发生氧化还原反应,它能使酸性高锰酸钾溶液褪色,故A正确; B.避蚊胺中不含-COOH或-OH,不能发生酯化反应,故B错误; C.避蚊胺中含有N元素,不属于烃,它与甲苯不是同系物,故C错误; D.避蚊胺含有苯环,一定条件下,它可与H2发生加成反应,故D正确. 故答案为:A、D; (2)根据有机物的结构和官能团之间的转化可知②③④⑤为取代反应,故答案为:②③④⑤; (3)对比C和DEET的结构可知C生成DEET的反应为取代反应,方程式为 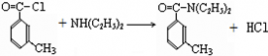 ,E为  ,氧化可生成  ,反应的方程式为  , 故答案为: 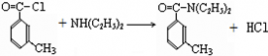 ;  ; (4)E为  ,同分异构体能与FeCl3溶液发生显色的反应,说明含有酚羟基,且结构中不含乙基,则应含有2个甲基,可能的结构简式为  , 故答案为:  (任写2种); (5)A为  ,A的某种同分异构体J只有两个吸收峰,说明J中的甲基应位于对位,为1,4二甲基苯或对二甲苯, 酸性高锰酸钾氧化后得到 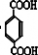 ,与乙二醇发生缩聚反应,方程式为 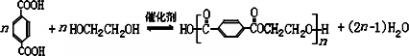 , 故答案为:1,4二甲基苯或对二甲苯;  . |
考点:
考点名称:有机物的合成有机物的合成: 的碱性水解等。
的碱性水解等。 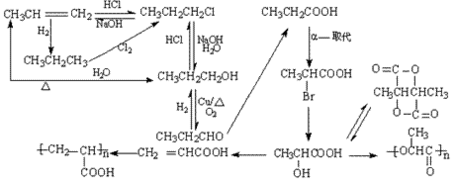


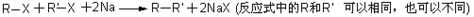
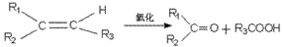
三 : 苯丙酸诺龙是一种兴奋剂,结构简式为(1)由苯雨酸诺龙的结构推测,它能__________(填代号)。
| 苯丙酸诺龙是一种兴奋剂,结构简式为 |
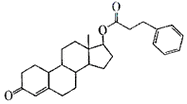 |
| (1)由苯雨酸诺龙的结构推测,它能__________(填代号)。 a.使溴的四氯化碳溶液褪色 b.使酸性KMnO4溶液褪色 c.与银氨溶液发生银镜反应 d.与Na2CO3溶液作用生成CO2 苯丙酸诺龙的一种同分异构体A,在一定条件下可发生下列反应: |
 |
提示:已知反应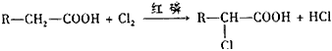 |
| 据以上信息回答(2)~(4)题: (2)B→D的反应类型是________________。 (3)C的结构简式为__________。 (4)F→G的化学方程式是______________。 |
| (1) ab (2)加成反应(或还原反应) |
(3)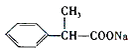 (4)  |
考点:
考点名称:有机物的推断有机物推断的一般方法: 的量,确定分子中不饱和键的类型及数目;由加成产物的结构,结合碳的四价确定不饱和键的位置。
的量,确定分子中不饱和键的类型及数目;由加成产物的结构,结合碳的四价确定不饱和键的位置。 根据反应现象推知官能团:
①能使溴水褪色,可推知该物质分子中可能含有碳碳双键、三键或醛基。
②能使酸性高锰酸钾溶液褪色,可推知该物质分子中可能含有碳碳双键、三键、醛基或为苯的同系物。
③遇三氯化铁溶液显紫色,可推知该物质分子含有酚羟基。
④遇浓硝酸变黄,可推知该物质是含有苯环结构的蛋白质。
⑤遇I2水变蓝,可推知该物质为淀粉。
⑥加入新制氢氧化铜悬浊液,加热,有红色沉淀生成;或加入银氨溶液有银镜生成,可推知该分子结构有-CHO即醛基。则该物质可能为醛类、甲酸和甲酸某酯。
⑦加入金属Na放出H2,可推知该物质分子结构中含有-OH或-COOH。
⑧加入NaHCO3溶液产生气体,可推知该物质分子结构中含有-COOH或-SO3H。
⑨加入溴水,出现白色沉淀,可推知该物质为苯酚或其衍生物。
根据物质的性质推断官能团:
能使溴水褪色的物质,含有C=C或C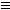 C或-CHO;能发生银镜反应的物质,含有-CHO;能与金属钠发生置换反应的物质,含有-OH、-COOH;能与碳酸钠作用的物质,含有羧基或酚羟基;能与碳酸氢钠反应的物质,含有羧基;能水解的物质,应为卤代烃和酯,其中能水解生成醇和羧酸的物质是酯。但如果只谈与氢氧化钠反应,则酚、羧酸、卤代烃、苯磺酸和酯都有可能。能在稀硫酸存在的条件下水解,则为酯、二糖或淀粉;但若是在较浓的硫酸存在的条件下水解,则为纤维素。
C或-CHO;能发生银镜反应的物质,含有-CHO;能与金属钠发生置换反应的物质,含有-OH、-COOH;能与碳酸钠作用的物质,含有羧基或酚羟基;能与碳酸氢钠反应的物质,含有羧基;能水解的物质,应为卤代烃和酯,其中能水解生成醇和羧酸的物质是酯。但如果只谈与氢氧化钠反应,则酚、羧酸、卤代烃、苯磺酸和酯都有可能。能在稀硫酸存在的条件下水解,则为酯、二糖或淀粉;但若是在较浓的硫酸存在的条件下水解,则为纤维素。
(4)根据特征数字推断官能团
①某有机物与醋酸反应,相对分子质量增加42,则分子中含有一个-OH;增加84,则含有两个-OH。缘由-OH转变为
-OOCCH3。
②某有机物在催化剂作用下被氧气氧化,若相对分子质量增加16,则表明有机物分子内有一个-CHO(变为-COOH);若增加32,则表明有机物分子内有两个-CHO(变为-COOH)。
③若有机物与Cl2反应,若有机物的相对分子质量增加71,则说明有机物分子内含有一个碳碳双键;若增加142,则说明有机物分子内含有二个碳碳双键或一个碳碳叁键。
根据反应产物推知官能团位置:
①若由醇氧化得醛或羧酸,可推知-OH一定连接在有2个氢原子的碳原子上,即存在-CH2OH;由醇氧化为酮,推知-OH一定连在有1个氢原子的碳原子上,即存在 ;
;
若醇不能在催化剂作用下被氧化,则-OH所连的碳原子上无氢原子。
②由消去反应的产物,可确定-OH或-X的位置
③由取代反应产物的种数,可确定碳链结构。如烷烃,已知其分子式和一氯代物的种数时,可推断其可能的结构。有时甚至可以在不知其分子式的情况下,判断其可能的结构简式。
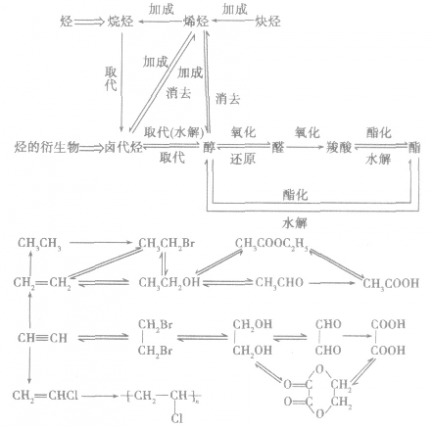
④由加氢后碳链的结构,可确定原物质分子C=C或C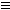 C的位置。
C的位置。
根据反应产物推知官能团的个数:
①与银氨溶液反应,若1mol有机物生成2mol银,则该有机物分子中含有一个醛基;若生成4mol银,则含有二个醛基或该物质为甲醛。
②与金属钠反应,若1mol有机物生成0.5molH2,则其分子中含有一个活泼氢原子,或为一个醇羟基,或酚羟基,也可能为一个羧基。
③与碳酸钠反应,若1mol有机物生成0.5molCO2,则说明其分子中含有一个羧基。
④与碳酸氢钠反应,若1mol有机物生成1molCO2,则说明其分子中含有一个羧基。
根据反应条件推断反应类型:
①在NaOH水溶液中发生水解反应,则反应可能为卤代烃的水解反应或酯的水解反应。
②在氢氧化钠的醇溶液中,加热条件下发生反应,则一定是卤代烃发生了消去反应。
③在浓硫酸存在并加热至170℃时发生反应,则该反应为乙醇的消去反应。
④能与氢气在镍催化条件下起反应,则为烯、炔、苯及其同系物、醛的加成反应(或还原反应)。
⑤能在稀硫酸作用下发生反应,则为酯、二糖、淀粉等的水解反应。
⑥能与溴水反应,可能为烯烃、炔烃的加成反应。
根据反应类型推断官能团:
利用官能团的衍生关系进行衍变(从特定的转化关系上突破):
(1)
(2)芳香化合物之间的相互转化关系
其他不常见有机物(杂环、难命名的有机物、K粉)
(1)根据有机物结构简式计算消耗碱的量:
①1mol酚羟基消耗1mol氢氧化钠;
②1mol羧基消耗1mol氢氧化钠;
③若有酯的结构,则先让酯进行酸性水解,再看产物能否和氢氧化钠反应:若酸性水解的产物是羧酸和醇,1mol酯只能和1mol氢氧化钠反应;若酸性水解的产物是羧酸和酚类物质,则1mol酯能和2mol氢氧化钠反应
(2)根据有机物结构简式写出其分子式
①如果题目给出了有机物结构的球棍模型,我们首先要判断每个球各代表何种元素的原子,它们之间是以单键、双键还是叁键结合的,此时各原子可采用数的办法以确定其个数。
如:某有机物分子结构模型为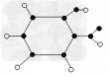 经观察易知:六元环为苯环,且为苯的邻二代物,分别是羟基和醛基,则其分子式为:C7H6O2。
经观察易知:六元环为苯环,且为苯的邻二代物,分别是羟基和醛基,则其分子式为:C7H6O2。
②利用不饱和度确定氢原子的个数,如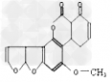
共有18个C:6+6+1+1+4=18,若饱和,H原子应为2×18+2=38(个)。不饱和度:除苯环外另有四个环,碳碳双键和碳氧双键各两个,所以不饱和度为4+4+2+2=12,故H原子的个数为:38-12×2=14,其分子式为C18H14O6
根据此原则,有机物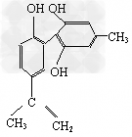
该有机物的C原子数为1+6+6+3=16,不饱和度为9。所以H原子数为16×2+2-9×2=16,其分子式为C16H16O3。
(3)若烃或烃的含氧衍生物中出现-X或-NO2,由于-X和-NO2均是取代一个H原子,所以-X或-NO2每增加一个,对应的H原子就少一个。
如: C原子数为14,不饱和度为7,另有两个Cl原子,则H原子数为14×2+2-7×2-2×1=14,即分子式为C14H14Cl2O4。
C原子数为14,不饱和度为7,另有两个Cl原子,则H原子数为14×2+2-7×2-2×1=14,即分子式为C14H14Cl2O4。
又如: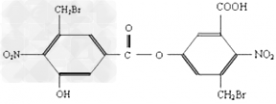 C原子数为16,不饱和度为1+4+1+4=10,-NO2和-Br各两个,所以H原子数为16×2+2-10×2-2×1-2×1=10,即分子式为C16H10N2O9Br2。
C原子数为16,不饱和度为1+4+1+4=10,-NO2和-Br各两个,所以H原子数为16×2+2-10×2-2×1-2×1=10,即分子式为C16H10N2O9Br2。
(4)据C、O、N三种元素原子的成键规律可知:在C原子数不变时,引入O原子,无论是-O-或-OH或羰基等,都不会影响到H原子的个数;而以-NH2或-NH-的形式引入N原子,则每多一个N原子对应就多一个H原子。
如: 其C原子数为17,不饱和度为4+2+3=9;-NO2为1、-NH-也为1,所以H原子数为17×2+2-9×2-1+1=18,即分子式为C17H18N2O6。
其C原子数为17,不饱和度为4+2+3=9;-NO2为1、-NH-也为1,所以H原子数为17×2+2-9×2-1+1=18,即分子式为C17H18N2O6。
四 : 巴豆酸的结构简式为CH3CH=CHCOOH,现有:①氯化氢②溴水③纯碱溶液④酸性KMnO4溶液⑤乙醇
| 巴豆酸的结构简式为CH3CH=CHCOOH,现有:①氯化氢 ②溴水 ③纯碱溶液 ④酸性KMnO4溶液 ⑤乙醇。在一定条件下能与巴豆酸反应的物质组合是 |
| [ ] |
| A.②④⑤ B.①③④ C.①②③ D.①②③④⑤ |
| D |
考点:
考点名称:羧酸的通性羧酸:
1.概念:烃基跟羧基相连构成的有机化合物叫做羧酸。一元羧酸的通式为 饱和一元羧酸的通式为
饱和一元羧酸的通式为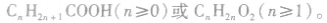
2.羧酸的分类:根据分子中烃基种类的不同,羧酸可分为脂肪酸和芳香酸等。分子中羧基与脂肪烃基相连的羧酸称为脂肪酸,如乙酸、硬脂酸;分子中羧基直接与苯环相连的羧酸称为芳香酸,如苯甲酸。
根据分子中羧基数目的不同,羧酸可分为一元羧酸、二元羧酸和多元羧酸等。分子中有一个羧基的羧酸称为一元羧酸,如乙酸;分子中有两个羧基的羧酸称为二元羧酸,如乙二酸(HOOC—COOH,俗称草酸)、对苯二甲酸
在一元羧酸里,酸分子的烃基含较多碳原子的称为高级脂肪酸,硬脂酸(C17H35COOH)、软脂酸(C15H31COOH)、油酸(C17H33COOH)都是常见的高级脂肪酸。
羟酸的性质:
1、羧酸的物理性质:
分子中碳原子数在4以下的羧酸能与水互溶。随着分子中碳链的增长,羧酸在水中的溶解度减小,直至与相对分子质量相近的烷烃溶解度相近。
羧酸分子间可以形成氢键。羧基中有两个氧原子,既可以像醇分子那样通过羟基氧和羟基氢形成氢键,也可以通过羰基氧和羟基氢形成氢键。由于羧酸分子形成氢键的机会比相对分子质量相近的醇多,所以羧酸的沸点比相应醇的沸点高。例如,乙酸和1一丙醇的相对分子质量都是60,但乙酸的沸点为117.9℃, 1一丙醇的沸点为97.2℃。
2、羧酸的化学性质
羧基由羰基和羟基组成,由于官能团之间的相互影响,使得羧酸的化学性质并不是羟基具有的化学性质和羰基具有的化学性质的简单加和。与醇羟基相比,羧基中羟基上的氢原子更易以离子形式电离出来,所以羧酸有酸性。与醛、酮的羰基相比,羧基中的羰基较难发生加成反应。羧酸很难通过催化加氢的方法被还原,用强还原剂如LiAlH4时才能将羧酸还原为相应的醇。
羧酸的主要化学性质如下:
(1)酸性
羧酸为弱电解质,羧酸、碳酸、苯酚的酸性由强到弱的顺序是: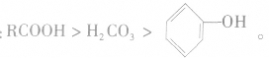 具有酸的通性。
具有酸的通性。 
(2)酯化反应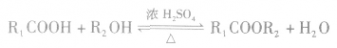
酯化反应也属于取代反应的范畴。酯化反应是制备酯的一种常用方法。
(3)形成酸酐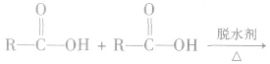

酸酐(羧酸分子间脱水的产物)可向有机化合物分 子提供酰基( ),是良好的酰化试剂。
),是良好的酰化试剂。
5.重要的羧酸
(1)甲酸
甲酸的结构式为 ,分子中既有羧基又有醛基,所以甲酸既有羧酸的化学性质(如弱酸性、发生酯化反应),又有像醛一样的还原性(如被银氨溶液和新制氢氧化铜悬浊液氧化)。甲酸是组成最简单的羧酸,最早是从蚂蚁体内提取出来的,故又称蚁酸。甲酸是有刺激性气味的无色液体,有腐蚀性,能与水、乙醇、乙醚、甘油等互溶。甲酸在工业上可用作还原剂,在医疗上可用作消毒剂。
,分子中既有羧基又有醛基,所以甲酸既有羧酸的化学性质(如弱酸性、发生酯化反应),又有像醛一样的还原性(如被银氨溶液和新制氢氧化铜悬浊液氧化)。甲酸是组成最简单的羧酸,最早是从蚂蚁体内提取出来的,故又称蚁酸。甲酸是有刺激性气味的无色液体,有腐蚀性,能与水、乙醇、乙醚、甘油等互溶。甲酸在工业上可用作还原剂,在医疗上可用作消毒剂。
(2)乙酸
乙酸俗称醋酸,通常为无色液体,具有强烈的刺激性气味,沸点117.9℃,熔点16.60C。当温度低于 16.60c时,乙酸就凝结成像冰一样的晶体,所以纯净的乙酸又称冰醋酸。乙酸是一种重要的有机化工原料,用途极为广泛。乙酸可用于生产醋酸纤维、合成纤维(如维纶)、喷漆溶剂、香料、染料、医药以及农药等。乙酸还是人们生活中的调味剂,普通食醋中含3%~5%(质量分数)的乙酸。
目前工业上合成乙酸的主要方法是乙醛氧化法,即用醋酸锰为催化剂,用氧气或空气作氧化剂氧化乙醛生成乙酸。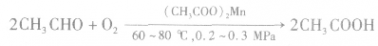
氢原子活性与物质的性质:
醇、酚、羧酸的结构中均有一OH,可分别称之为 “醇羟基”“酚羟基”和“羧羟基”。由于与这些一OH相连的基团不同,一OH受相连基团的影响就不同。故羟基上的氢原子活性也就不同,表现在性质上也相差较大,可比较如下: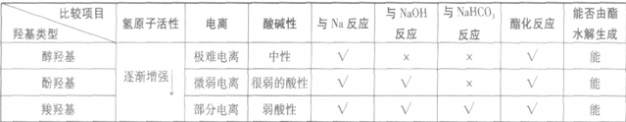
烯烃的通性:
(1)物理性质:随着分子中碳原子数的递增,熔沸点逐渐升高,相对密度逐渐增大,常温下存在状态,由气态逐渐过渡到液态、固态。
(2)化学性质:烯烃可发生氧化、加成、加聚等反应。
①烯烃的氧化反应:烯烃燃烧生成二氧化碳和水。CnH2n+3n/2O2 nCO2+nH2O
nCO2+nH2O
②烯烃的加成:烯烃可与氢气、卤素单质、水、卤化氢等发生加成反应。烯烃的加聚反应:以乙烯为例: ,加聚时碳碳双键打开。
,加聚时碳碳双键打开。
③二烯烃的加成反应:以1,3-丁二烯(CH2=CH-CH=CH2)加成为例
1,2加成就是加成普通的不饱和键,和普通的烯烃和炔烃的加成一样。与氯气加成:CH2=CH-CH=CH2+Cl2→CH2Cl-CHCl-CH=CH2
1,4加成,1,4加成是分别加成两边的2个不饱和键,然后在中间重新形成一个双键。与氯气加成:CH2=CH-CH=CH2+Cl2→CH2Cl-CH=CHCH2Cl
(3)烯烃的顺反异构:根据在两个由双键连接的碳原子上所连的四个原子或基团中两个相同者的位置来决定异构体的类型。当两个相同的原子或基团处于π键平面的同侧时称“顺式异构(cis-isomerism)”;当处于π键平面的异侧时称“反式异构(trans-isomerism)”。Z表示顺,E表示反。 
五 : 巴豆酸的结构简式为:CH3—CH=COOH。试回答:
巴豆酸的结构简式为:CH3—CH=COOH。试回答:
1.巴豆酸的分子中含有____和____两种官能团(写名称);
2.巴豆酸与金属钠反应的化学方程式为:
3.巴豆酸___(填“能”或“不能”)使KMnO4(H+)褪色。
(www.61k.com)4.巴豆酸跟乙醇在浓硫酸催化下发生酯化反应的化学方程式为:
5.巴豆酸与溴水反应的化学方程式为:
你写的结构不对
 本文标题:巴豆酸的结构简式为-巴豆酸的结构简式为CH3CH=CHCOOH ,现有①水;②溴的四氯化碳溶液;③乙醇;④纯碱溶液;能与之反应的?
本文标题:巴豆酸的结构简式为-巴豆酸的结构简式为CH3CH=CHCOOH ,现有①水;②溴的四氯化碳溶液;③乙醇;④纯碱溶液;能与之反应的? 61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1